12 лютого Міністерство охорони здоров'я (МОЗ) України провело зустріч з представниками бізнесу та партнерами для обговорення євроінтеграційних ініціатив у фармацевтичному секторі.
На зустрічі представники фармспільноти отримали інформацію про результати перемовин МОЗ з європейськими країнами та міжнародними регуляторними органами. Особливу увагу приділили питанням реформування фармацевтичного регуляторного органу, гармонізації законодавства з нормами права ЄС, а також проблемі антимікробної резистентності.
Євроінтеграційна стратегія у фармацевтичному секторі має 8 визначених цілей:
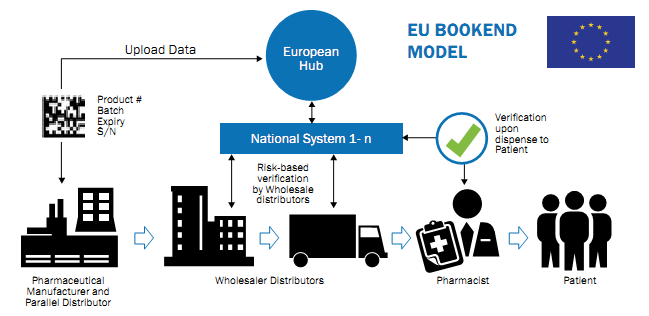
- Гармонізація законодавства України з нормами права ЄС. У фармацевтичній галузі необхідно внести зміни у закон про лікарські засоби та низку інших законодавчих актів, що регулюють державну реєстрацію та впровадження стандарту передачі технічної нормативної документації (eCTD), доклінічні та клінічні випробування, фармаконагляд, верифікацію лікарських засобів з 2D-кодуванням; а також низку законів та регламентів, що регулюють медичні вироби.
- Реформування фармацевтичного регуляторного органу. Зараз в Україні створюють центральний орган виконавчої влади, що відповідатиме за реєстрацію та контроль за ринком ліків, медвиробів та косметики. Новий регуляторний орган створить чіткі правила гри для всіх учасників ринку, а також забезпечить вищу якість, безпечність та доступність ліків.
- Локалізація фармацевтичних виробництв в Україні. Створення в нашій країні майданчиків для виробництва іноземних ліків сприятиме залученню інвестицій у фармацевтичну галузь та створенню нових робочих місць.
- Наявність та доступність ліків. В Україні це залежить не лише від вітчизняного виробника, а й від імпорту. Для цього процеси реєстрації ліків та підтвердження сертифікатів GMP (відповідності умов виробництва міжнародним стандартам) мають бути прозорими і швидкими.
- Стійкість до антимікробних препаратів. Боротьба з антибіотикорезистентністю та забезпечення ефективного використання антибіотиків необхідна для того, щоб ми і далі могли успішно лікувати бактеріальні та грибкові інфекції, безпечно приймати пологи, проводити оперативні втручання тощо.
- Розвиток клінічних випробувань. Ми прагнемо, щоб інші країни проводили клінічні випробування лікарських препаратів в Україні. Для цього важливо посилювати комунікацію та залучення інноваційних фармвиробників до співпраці з українськими клінічними базами. Проведення інспектування клінічних випробувань зі сторони міжнародних партнерів додатково підкреслить прозорість і відповідальність процесів в Україні та дотримання етичних принципів.
- Цифрова інтеграція з ЄС. Це дозволить Україні доєднатися до європейських баз даних та сприятиме впровадженню сучасних технологій та стандартів управління фармацевтичними процесами.
- Доступ до ринку ЄС. Цей пункт передбачає відкриття нових можливостей для експорту українських лікарських засобів на європейський ринок. Для цього нам потрібно гармонізувати регуляторне середовище з ЄС, підписати угоди про оцінку відповідності та прийнятності промислових товарів та домовитися про взаємне визнання GMP-сертифікатів.
«Ми постійно спілкуємось з представниками бізнесу та міжнародними партнерами. Для нас важлива їх позиція, тому ми відкриті до обговорення будь-яких питань. Зараз Єврокомісія розпочала скринінг українського законодавства щодо його рівня імплементації директив і регламентів Європейського Союзу. Україна вже отримала звіт за результатами внутрішньої перевірки законодавства. На основі звіту розроблений план на виконання рекомендацій Єврокомісії. Євроінтеграційні процеси в Україні є невідворотними. Наша країна активно рухається в цьому напрямі, і в сфері охорони здоровʼя зокрема», — зауважив міністр охорони здоров’я Віктор Ляшко.
МОЗ та інші міністерства та відомства продовжують працювати з представниками Європейської комісії, щоб українське законодавство відповідало нормам ЄС, а також співпрацювати з іншими європейськими агенціями у всіх вищезазначених сферах. У цьому процесі активну участь беруть фармацевтичні підприємства, аптечні мережі та інші учасники ринку, адже український фармацевтичний сектор є однією з найпотужніших та найконкурентніших галузей економіки країни, яка має гарні перспективи швидко інтегруватися у ЄС.
«Стратегічне бачення наших євроінтеграційних процесів у фармацевтичній сфері вибудувано таким чином, щоб забезпечити збереження людського капіталу та, як наслідок, — економічний розвиток країни. І саме фармацевтична галузь є двигуном економічного зростання», - наголосила заступниця Міністра охорони здоров'я України з питань європейської інтеграції Марина Слободніченко.
Зустріч проведена за сприяння проєкту «Безпечні, доступні та ефективні ліки для українців» (SAFEMed), який фінансується Агентством США з міжнародного розвитку (USAID).