Торстен Цех1, Моника Хаберехт2, Тиль Грюндлинг3, Бастиан Штаал3, Андреас Грюцке2,4
1БАСФ СЕ, Европейская Прикладная Лаборатория (PharmaSolutions), Людвигсхафен (Германия).
2БАСФ СЕ, Глобальный технический маркетинг и управление продуктами, Людвигсхафен (Германия).
3БАСФ СЕ, Экспертно-консультационный центр по аналитической работе, Определение структурных характеристик полимеров, Людвигсхафен (Германия).
4теперь в AbbVie Germany GmbH & Co., Process Engineering Sciences NCE, Людвигсхафен (Германия).
Ответственный автор: thorsten.cech@basf.com
Введение
Полиоксил касторовое масло (ПЭГ-40 гидрогенизированное касторовое масло) представляет собой неионный солюбилизатор и эмульгатор, получаемый при взаимодействии 1 моля гидрогенизированного касторового масла с 40 молями этиленоксида. Основными составляющими вспомогательного вещества являются гидроксистеарат глицерина и полиэтиленгликоля, которые вместе с полигликолевыми эфирами жирных кислот и глицерина образуют гидрофобную часть продукта. Гидрофильная часть состоит из полиэтиленгликолей и глицерина этоксилата.
Вспомогательное вещество описано во всех основных Фармакопеях:
• Британская Фармакопея: Hydrogenated Polyoxyl Cator Oil (гидрогенизированное полиоксил касторовое масло)
• Европейская Фармакопея: Macrogolglycerol Hydroxystearate (полиэтиленгликоля глицерингидростеарат)
• Фармакопея США – Национальный формуляр: Polyoxyl 40 Hydrogenated Castor Oil (полиоксил 40 гидрогенизированное касторовое масло).
Полиоксил касторовое масло применяют преимущественно в качестве солюбилизатора и/или эмульгатора в жидких и мягких лекарственных формах для перорального и местного применения (например, LBDDS, SEDDS). Поскольку полиоксил касторовое
масло по своей природе содержит смесь различных химических веществ, оно не имеет четкой точки плавления, но плавится в довольно широком диапазоне от -16 до +26 °C.
Цель
Цель данного исследования – изучить потенциальную потребность в плавлении и гомогенизации продукта перед использованием. Соответственно в публикации обсуждено, возникают ли критичные свойства материала (КСМ), если продукт не гомогенизирован перед отбором проб.
Материалы и методы
Полиоксил касторовое масло (Kolliphor® RH 40, BASF) испытывали в оригинальных коммерческих барабанах, каждый по 60 кг. Каждый барабан обрабатывали по-разному в соответствии со следующим описанием:
• Барабан A: замороженный, не гомогенизированный
Весь барабан замораживали при -18 °C и хранили при указанной температуре в течение 1 недели. Затем весь барабан разрезали на три части, что позволило провести индивидуальное аналитическое исследование верхней, средней и нижней секций наполнителя для оценки его однородности.
• Барабан B: расплавленный, не гомогенизированный
Весь барабан расплавляли при 40 °C и хранили при указанной температуре в течение 1 недели. Затем барабан открывали и тщательно отбирали образцы наполнителя, представляющие верхнюю, среднюю и нижнюю секцию, чтобы предотвратить перекрестное перемешивание или гомогенизацию.
• Барабан C: расплавленный, гомогенизированный
Весь барабан расплавили при температуре 40 °C, а затем открыли. Наполнитель полностью интенсивно гомогенизировали (посредством перемешивания), затем отобрали образец и предоставили его для аналитического исследования в качестве эталона. Кроме того, образцы (n=3) прошли испытание при качании. Полиоксил касторовое масло расплавляли при температуре 65 °C и выдерживали при 60 °C в течение 5 дней. По истечении этого периода полученный продукт охлаждали для затвердевания при комнатной температуре и хранили в данных условиях в течение 24 ч. Весь цикл повторяли 20 раз. После этого образцы предоставляли для аналитического исследования, а результаты сопоставляли с исходными значениями.
Характеристики полиоксил касторового масла согласно фармакопейным статьям в действующих Фармакопеях: температура застывания, кислотное число, гидроксильное число, йодное число, значение омыления, содержание воды, а также сульфатной золы. Все указанные испытания проводили с применением фармакопейных методов.
Дифференциальная сканирующая калориметрия (ДСК)
Использовали аппарат DSC Q2000 V24.4 Build 116 и образцы массой от 8 до 9 мг. После быстрого охлаждения до -80 °C температуры плавления (Tm) определяли при скорости нагрева 20 K/мин (n=2) в диапазоне температур от -80 до +85 °C. Проводили два цикла, оценивали значения второго цикла (Tm2).
Эксклюзионная хроматография по размеру (ЭХР)
Разделение методом ЭХР выполняли на системе Agilent 1200 для высокоэффективной жидкостной хроматографии (ВЭЖХ), состоящей из дегазатора растворителя, четвертичного насоса для сверхэффективной жидкостной хроматографии (СЭЖХ), автоматического пробоотборника, подогреваемого колоночного отделения, показателя преломления и УФ-детектора с переменной длиной волны. Калибровку проводили с использованием стандартов полиэтиленгликоля с низкой полидисперсностью (PolymerLabs).
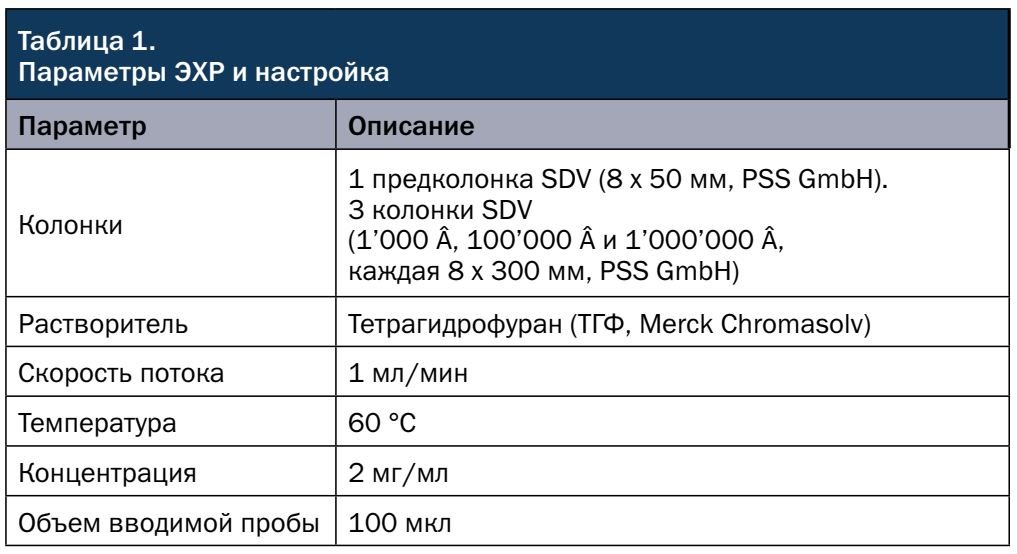
Образцы растворяли в элюенте ЭХР, полученные растворы пропускали через шприцевой фильтр (ChromafilXtra PTFE, 0,20 мкм) перед введением (табл. 1).
Время-пролетная ионизация лазерной десорбцией с использованием матрицы
Спектры получали в режиме положительного отражателя на масс - спектрометре Bruker ultrafleXtreme MALDI. Образцы готовили методом растворения/измельчения, так как этот метод дает более воспроизводимые спектральные данные, чем приготовление жидких капель. Кончик шпателя с матрицей (транс-2-[3-(4-третбутилфенил)-2-метил-2-пропенилиден] малононитрил, DCTB) добавляли в небольшую агатовую ступку вместе с ок. 10 мкл раствора NaCl (0,1 моль/л в H2O).
Матрицу и солевой раствор измельчали до получения мелкозернистой пасты. Впоследствии добавляли ок. 10 мкл раствора образца (10 мг/мл в ТГФ) и смесь измельчали еще в течение нескольких секунд. Пасту наносили в виде очень тонкой пленки на стальную шлифованную мишень с помощью пластикового шпателя.
 Результаты и обсуждение
Результаты и обсуждение
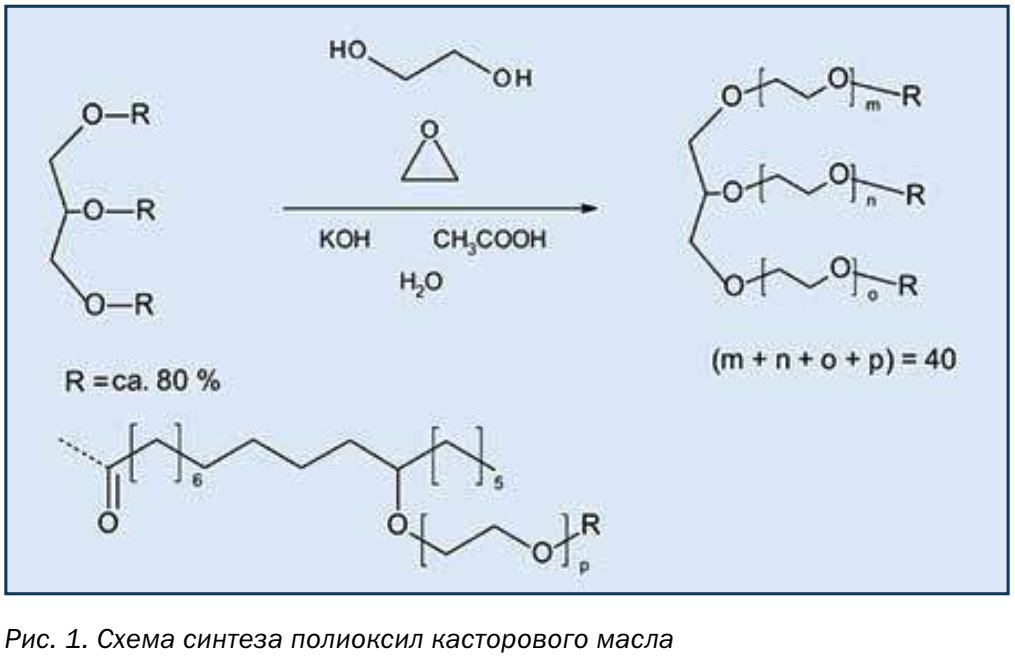
Полиоксил касторовое масло – это продукт на натуральной основе, полученный посредством химической реакции гидрогенизированного касторового масла с этиленоксидом (рис. 1). Конечное вспомогательное вещество состоит из нескольких различных компонентов. Разнообразие составляющих компонентов продукта обусловливает его превосходные функциональные возможности в качестве солюбилизатора. С точки зрения критериев качества через разработку, КСМ могут возникнуть из-за различий в целостности или однородности продуктов.
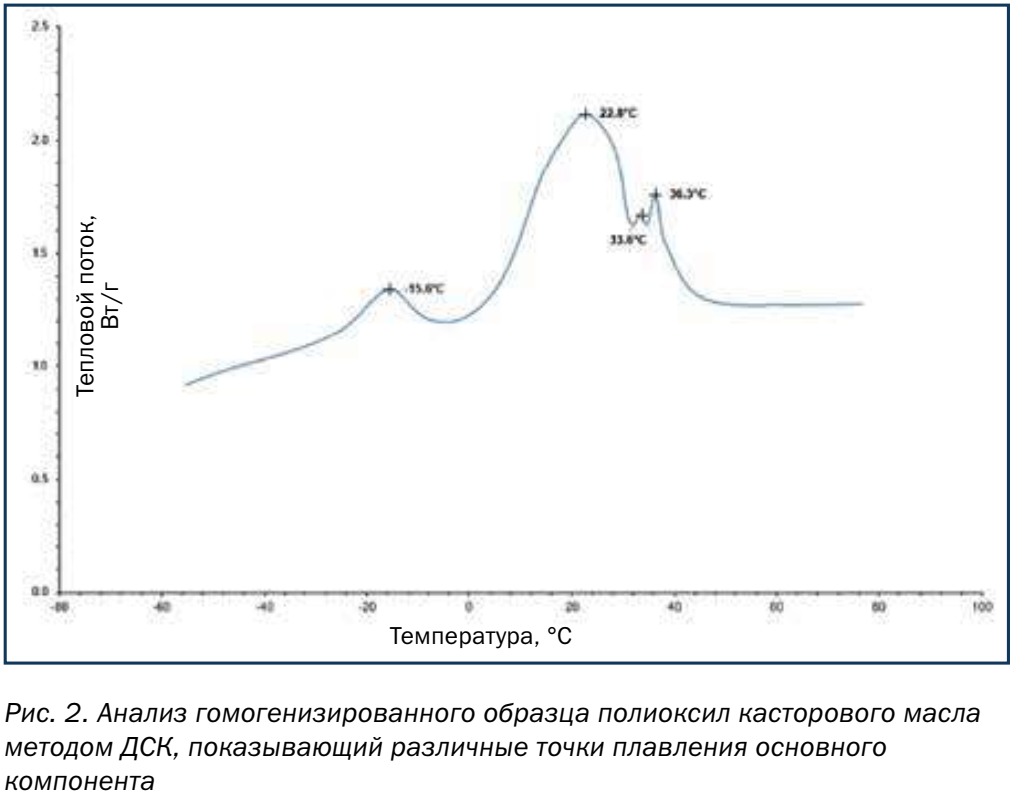
Следовательно, как показывает анализ методом ДСК, наличие нескольких компонентов продукта приводит к широкому диапазону температур плавления продукта – от -16 до +26 °C (рис. 2). Точка плавления одного компонента при температуре около -16 °C является основным условием полутвердого вида продукта в условиях окружающей среды. При температуре около +26 °C основная фракция плавится/затвердевает, что соответствует верхнему пределу диапазона плавления, указанному в литературе. Продукт выглядит постоянно жидким во время хранения при температуре выше +26 °C. Однако анализ методом ДСК свидетельствует о наличии также компонентов с более высокой температурой плавления, которые плавятся в диапазоне температур от +33 до +38 °C.
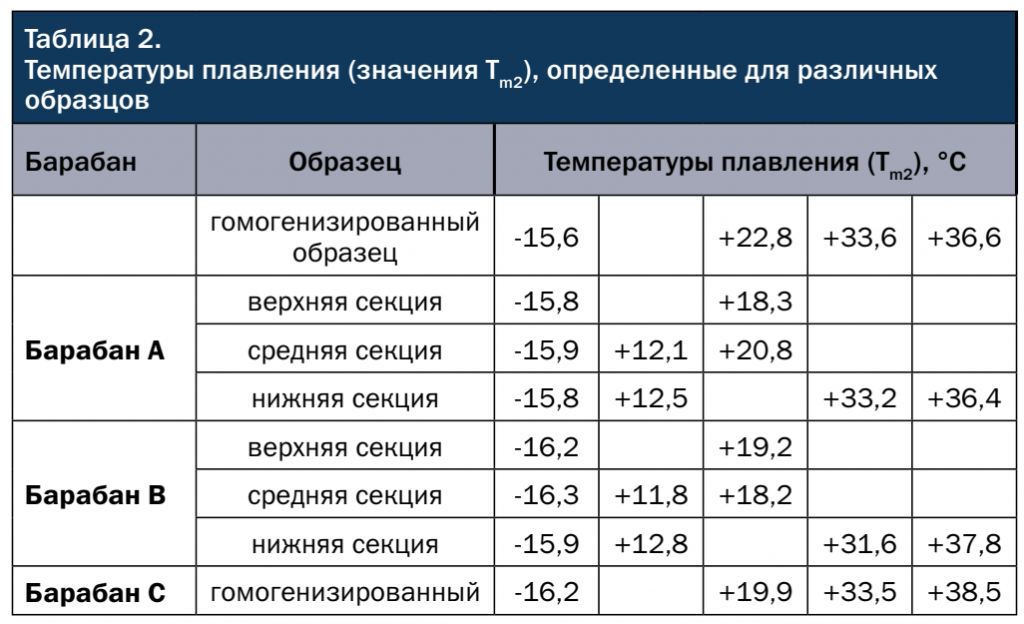
Предполагая, что разные температуры плавления представляют разные основные компоненты продукта, однородность можно оценить с помощью анализа методом ДСК. Для этого из различных секций барабанов взяли образцы для испытания с помощью метода ДСК (табл. 2). Оба аспекта, отсутствие пика плавления или менее выраженное начало, могут указывать на то, что соответствующий компонент либо не содержится, либо просто присутствует в более низкой концентрации.
Результаты, полученные при использовании гомогенизированного барабана C, соответствовали температурам плавления, определенным для эталонного образца (рис. 2), что свидетельствует о надлежащей однородности продукта. По-другому выглядят результаты для барабана A и барабана B. В процессе замораживания фракции, имеющие более высокую температуру плавления, сначала затвердевают и начинают оседать в оставшемся жидком продукте. Это можно увидеть, если налить полиоксил касторовое масло в стеклянную колбу при температуре 40 °C, а затем дать ей остыть (рис. 3).
Из-за этого осаждения компоненты с более высокой температурой плавления сосредоточиваются в нижней секции барабана. Учитывая это, продукт следует расценивать как неоднородный во время хранения при комнатной температуре. Результаты, полученные при использовании барабана B, показывают, что после плавления разделение компонентов сохранилось. Простое плавление без перемешивания продукта не приводит к достижению его однородности.

Анализ методом ЭХР может быть использован для доказательства того, что разделение основано на вариации молекулярной массы компонентов продукта. В диапазоне относительной молекулярной массы около 1000 г/моль можно обнаружить вариацию в зависимости от секции барабана, из которой был взят образец (рис. 4). Эти результаты подтверждены данными матрично-активированной лазерной десорбции/ионизации с масс-спектрометрией. Различия в образцах ясно указывали на различный состав фракций продукта (рис. 5). Данные время-пролетной ионизации лазерной десорбцией с использованием матрицы могут помочь понять химическую природу этих фракций (рис. 6 – 8). Продукты, перечисленные в табл. 3, являются наиболее вероятными компонентами. В отпечатке матрично-активированной лазерной десорбции/ионизации с масс-спектрометрией массспектральные интенсивности отображаются на графике как функция длины цепи и функциональной группы, а не отношения массы к заряду. Хотя отпечаток матрично-активированной лазерной десорбции/ионизации с масс-спектрометрией не является абсолютным количественным представлением состава образца, он позволяет проводить полуколичественное сравнение изменений от серии к серии в сложных многомерных распределениях гомологов, регулирующих продукты такого типа.
Состав различных образцов визуально отображен на диаграммах. Синие точки представляют разновидности, состоящие из глицерина, полиэтиленгликоля (ПЭГ) и гидроксистеариновой кислоты, тогда как зеленые – отображают разновидности, состоящие только из ПЭГ и гидроксистеариновой кислоты. На оси Y показано количество звеньев стеариновой кислоты, содержащихся в одной молекуле (молекулы: неэтерифицированные, моно-, ди-, три- и тетраэфиры, обозначенные увеличивающимся значением шкалы Y). Хорошо видно, что в смеси продуктов присутствуют частицы, содержащие до четырех групп гидроксистеариновой кислоты.
Сравнение различных диаграмм отпечатков матрично-активированной лазерной десорбции/ионизации с масс-спектрометрией четко визуализирует различия в проанализированных образцах. Эти различия наиболее отчетливо видны при сравнении верхней и нижней секций барабана А. Нижняя фракция показывает заметно большее количество свободного ПЭГ (зеленые точки на оси Х без гидроксистеариновой кислоты). Это обогащение свободного ПЭГ нельзя увидеть ни в верхних фракциях, ни в образцах гомогенизированного барабана.


