Фармацевтична галузь є однією з найважливіших для економіки кожної країни.
Під час Першої та Другої світових воєн у фармацевтичній галузі були періоди розвитку і відбулось багато визначних подій. Варто пригадати лише відкриття сульфаніламіду та пеніциліну в період між двома світовими війнами, що стало початком виробництва й розповсюдження ліків.
Розглядаючи ситуацію, в якій зараз перебуває українська фармацевтична галузь, та з огляду на історію становлення і розвитку фармринку, треба зауважити, що за жодних обставин не можна повністю зупиняти роботу. Навпаки, важливо зосередитись на розвитку інвестицій та інновацій, оскільки це значною мірою впливатиме на відновлення і розвиток країни в майбутньому.
Українські виробники мають забезпечувати населення якісними та доступними ліками за будь-яких обставин. Проаналізувавши список препаратів, яких наразі гостро потребують українці, можна зробити висновок, що вітчизняній фармі потрібно більше ефективних та доступних аналогів лікарських засобів-блокбастерів.
Сьогодні більше поговоримо про тверді форми ліків, оскільки вони найбільш зручні у використанні й мають стабільний попит у споживачів.
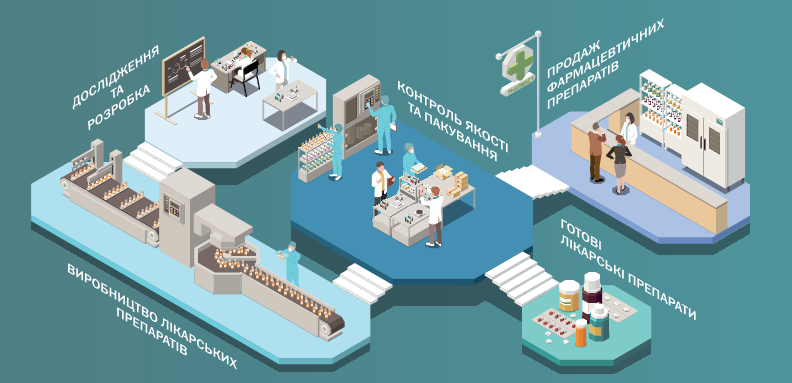
Будь-який продукт повинен пройти певний шлях від розробки до реалізації, кожен процес важливий для кінцевого результату та напряму, впливає на вартість і якість продукту.
Все починається з вибору та оцінки продукту, далі йде важли-вий етап пошуку та оцінки необхідних активних фармацевтичних інгредієнтів (АФІ) і матеріалів. На цьому етапі дуже цінним ресурсом є час, від якого залежить старт R&D-процесів. Сам R&D-процес є основою проєкту, потім відбуваються масштабування технології in-house або її трансфер на виробництво, дослідження стабільності лікарського засобу, його біоеквівалентності, підготовка до реєстрації та отримання реєстраційного посвідчення на продукт.
Фактори, які визначають життєвий цикл продукту, – це ініціація, якість і вартість проєкту.
Ініціація проєкту
Більшість виробників мають свої способи пошуку та оцінки тих продуктів, які зможуть гідно доповнити продуктовий портфель компанії. На підставі даних або результатів звітів відповідних установ можна розділити продукти на сегменти великого, середнього і малого обсягів продажу. До сегмента великого об’єму зазвичай відносять препарати для лікування серцево-судинних, цереброваскулярних, ортопедичних захворювань, цукрового діабету, антибактеріальні засоби тощо. Представниками цього сегмента найчастіше є препарати- блокбастери, які, попри високу вартість, затребувані серед споживачів. Аналоги ліків-блокбастерів необхідно випускати швидко, і є досить багато охочих це робити, тому що завдяки популярності продукту та обсягів його продажу компанія отримує не тільки економічну перевагу, а й набуває популярності. Зазвичай для досягнення такого результату фармацевтичному виробнику треба мати досвідчену R&D-команду, ресурси для швидкої підготовки проєкту та час, який є найважливішим ресурсом. Саме ліків цього сегмента нині бракує найбільше, і це великий поштовх для українських виробників – створювати аналоги для їхнього безперебійного постачання в аптечні заклади України.
Сегмент середнього і малого обсягів продажу представляють препарати для лікування психічних, гінекологічних захворювань, сечогінні засоби тощо. Обсяги продажу цих препаратів порівняно з таким великого сегмента відрізняються, але невеликим фармацевтичним компаніям варто зосередитись на одному-двох напрямах і працювати над розробкою та виробництвом нових лікарських препаратів в обраних категоріях.
Якість продукту
Якість препаратів залежить від дизайну проєкту. Візьмемо за приклад лікарські засоби у твердій формі – таблетки. Основні фактори, що впливають на вибір АФІ та плану розробки рецептур, серед яких оцінка ризику АФІ, є ключовою ланкою перед лабораторним дослідженням, контролем домішок АФІ, форми кристалів, розміру частинок тощо. Це впливатиме на стабільність таблетованих продуктів, їхнє розчинення in vitro, вивільнення, а також на результати дослідження біоеквівалентності.
Наразі все більше країн і фармацевтичних виробників приєднуються та підтримують міжнародну організацію з гармонізації технічних вимог ICH. Вимоги країн до якості ліків будуть ставати тільки жорсткішими, а напрямок управління і вимоги Європи та США є прикладом і тенденцією, які дають можливість випускати якісні продукти не тільки всередині країни, а й виходити на міжнародний ринок.
Вартість
Фактори, що впливають на загальну вартість: вартість R&D-процесу, вартість AФI, вартість виробництва.
Як розв'язати проблему собівартості та створити дійсно конкуренто-спроможний продукт? Одними з найважливіших складових вартості R&D-етапу є ефективність розробки й час. Для вирішення питання щодо вартості АФІ необхідно швидко налагодити стабільне постачання та винайти економічно ефективну фармацевтичну субстанцію. Зазначимо, що в даних умовах це дійсно не просто, але реально. Вартість виробництва залежить від обсягу партії.
Отже, підвищення ефективності досліджень і розробок та можливість знаходити економічно ефективні АФІ є ключовими моментами у загальному контролі витрат.
На кожному з етапів є труднощі, які можуть сповільнювати процеси реалізації проєкту. Сьогодні для максимально швидкого розвитку доцільно віддавати деякі процеси на аутсорсинг.
Розглянемо декілька питань та варіанти їхнього вирішення.
- Пошук і вибір АФІ. Часозатратний етап у проєкті, який потребує чимало ресурсів та напряму впливає на вартість і якість продукту. Вирішенням даного питання може стати аутсорсинг. Доцільно делегувати пошук потрібної речовини з опцією ретельної перевірки його якості за необхідними параметрами відповідно до вимог, що висуваються до проєкту, а також із подальшою можливістю проведення аудиту виробництва та перевірки реєстраційного досьє для майбутньої реєстрації. Завдяки цьому досягається економія часу на пошук, переговори, відправку зразка субстанції для перевірки якості, затребування документів та організацію відправки товару. Також перевагами є фінансова економія, гарантована якість і швидкість початку науково-дослідницьких робіт.
- Неможливість розробки лікарських засобів. У багатьох фармацевтичних компаніях проєкти перебувають «на паузі» та чекають кращих часів. Це дуже прикро, але, як ми зазначали вище, зупинка розвитку української фармацевтичної галузі є неприпустимою.
Вирішити це питання можна і завдяки партнерству з контрактно-дослідницькими організаціями. Доцільно розглянути як варіанти готових технологій, так і розробку на замовлення.
Плюси: швидкість реалізації проєкту, вирішення питань щодо пошуку та придбання АФІ, трансфер технології у будь-яку країну світу. Також компанії можуть розглянути варіант розробки і виробництва, якщо наразі у неї немає можливості виробляти продукт на своєму підприємстві, а згодом зробити трансфер уже на свій виробничий майданчик. Завдяки цьому робота компанії не зупиняється, є можливість продовжувати забезпечувати країну якісними та доступними ліками і, звісно, підтримувати економіку України.
Сьогодні як ніколи важливими є співпраця та партнерство для досягнення найкращого результату. Наша команда протягом двох років активно співпрацює з українськими фармацевтичними виробниками і ми продовжимо допомагати їм, і надалі. Швидко знаходимо варіанти допомоги та пропонуємо лояльні умови співпраці задля спільного майбутнього.
Tianjin Holder Pharmaceutical Technology Co., Ltd.
КНР, Тяньцзінь, Hengze Industrial Park, будівля 6
Тел.: +86 222 821 9283
Генеральний директор: Domy Wang
Комерційний директор: Діана Сальнікова
Тел.: +86 134 2625 5153