Дар'я Єдаменко
Дар'я Єдаменко
PhD, експертка з аналітичної хімії та Extractables & Leachables.
Має понад 15 років досвіду у фармацевтичних дослідженнях і розробках аналітичних методик (GC-MS, LC-MS, HPLC) та у впровадженні нових процесів, зокрема з оцінки E&L і координації міждепартаментних проєктів згідно з вимогами GMP, ICH та EMA/FDA.
https://www.linkedin.com/in/daria-yedamenko-ph-d-4483992b0/
У статті розглянуто зростаючу роль Extractables & Leachables (E&L) як критичного параметра дизайну та управління ризиками в процесі сучасного фармацевтичного пакування. У контексті ініціативи ICH Q3E, що перебуває на стадії Concept Paper, проаналізовано, як розвиток «зеленої» упаковки та матеріалів нового покоління впливає на формування аналітичної стратегії, підходи до вибору обладнання та валідації методик.
- Вступ: чому пакування = частина лікарського засобу?
Сучасне фармацевтичне пакування давно перестало бути лише «оболонкою» для готового продукту. Якщо раніше його розглядали переважно як фізичний захист і засіб стабільності, то сьогодні воно функціонально інтегроване в систему «лікарський засіб — контактуючий матеріал». Розвиток полімерних технологій, ускладнення складу лікарських форм та зростання регуляторних вимог привели до того, що пакування здатне суттєво впливати як на якість, так і на безпеку продукту.
Важливим чинником цього стали сучасні підходи до «зеленої» хімії та сталого розвитку, які активно впроваджують у процеси пакування фармацевтичної продукції. Використання перероблених і біоорієнтованих матеріалів, зменшення маси пакування, застосування нових багатошарових конструкцій та функціональних добавок формують нові можливості, але при цьому створюють додаткові виклики щодо хімічної сумісності. Отже, «зелена» упаковка не завжди означає автоматично безпечну, а перехід до використання матеріалів нового покоління потребує поглибленої оцінки потенційних хімічних ризиків.
Одним із ключових аспектів взаємодії лікарського засобу з пакувальними та іншими контактуючими матеріалами є профіль Extractables & Leachables (E&L) — потенційне вилуговування хімічних речовин у продукт. Абсолютна хімічна інертність таких матеріалів залишається радше теоретичним ідеалом, тому їхня взаємодія з лікарським засобом є очікуваною та має регулюватися на основі ризик-орієнтованого підходу, а не розглядатися виключно в межах аналітичного контролю домішок.
У сучасних підходах до оцінки сумісності лікарського засобу та контактуючих матеріалів Extractables розглядають як характеристику матеріалу, тоді як Leachables — як характеристику конкретного лікарського продукту за його реального застосування. Такий підхід дозволяє логічно пов’язати вибір пакувальних і технологічних матеріалів, умови контакту та етапи життєвого циклу продукту з обсягом, глибиною й послідовністю необхідних досліджень.
У цьому контексті оцінка E&L перестає бути завданням лише стадій досліджень стабільності — вона інтегрується в сам процес дизайну пакування: від вибору матеріалів і конструкції систем до вирішення технологічних питань виробництва. Сучасні вимоги, зокрема EU GMP Annex 1, підкреслюють необхідність застосування ризикорієнтованого підходу та впровадження комплексної Contamination Control Strategy (CCS) протягом усього життєвого циклу продукту.
2. ICH Q3E: що принципово змінилося
У фармацевтичній галузі триває робота над гармонізацією підходів до оцінки E&L. Наразі на стадії Concept Paper перебуває ініціатива ICH Q3E, яка має на меті створити єдину, науково обґрунтовану рамку для оцінки E&L, інтегровану в загальну систему ризик-орієнтованого регулювання.
На відміну від окремих рекомендацій чи технічних документів, Concept Paper ICH Q3E сигналізує про зсув регуляторної парадигми— від формальних досліджень до комплексного управління ризиками від самого початку розробки лікарського засобу.
Проєкт ICH Q3E також віддзеркалює тісний зв’язок з іншими важливими документами:
- ICH Q9— ризик-орієнтований підхід до якості;
- ICH Q12— управління життєвим циклом продукту;
- USP <665> / <1665>, <1663> /<1664>— стандарти оцінки E&L у лабораторних умовах.
Такий контекст суттєво впливає на різні групи учасників фармацевтичного ланцюжка:
- виробники пакування потребують ранньої оцінки ризиків сумісності матеріалів із продуктом;
- фармацевтичні компанії мають інтегрувати E&L у стратегії дизайну і контролю;
- QC-лабораторіям важливо адаптувати методики та підходи відповідно до очікувань ризик-орієнтованого регулювання.
Цей перехід у регуляторній логіці формує нові очікування щодо ролі пакування і вимагає від галузі перегляду традиційних підходів.
Отже, оцінка E&L стає одним із вихідних параметрів під час проєктування не лише пакувальної системи, але й вибору матеріалів для технологічного виробництва, визначаючи логіку вибору матеріалів і підходи до подальшого контролю протягом усього життєвого циклу лікарського засобу.
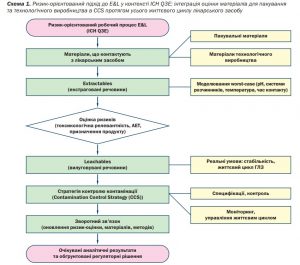
Узагальнену логіку ризик-орієнтованого підходу до E&L у контексті ICH Q3E, від вибору пакувальних і технологічних матеріалів до інтеграції в CCS, наведено на схемі 1.
3. E&L як параметр дизайну пакування
У сучасному підході до розроб-ки лікарських засобів E&L роз-глядають якодин із параметрівдизайну пакувальної системи, ане як ізольований етап контролю.Така логіка дозволяє враховуватипотенційні хімічні ризики вже наетапі проєктування та ухваленняінженерних рішень, а не лише настадії аналітичної оцінки готовогопродукту.
Полімерні матеріали таеластомери
Полімери та еластомери є ключовими компонентами як матеріалів технологічного виробництва так і первинного пакування та контейнерно-закупорювальних систем. Їхній хімічнийсклад, тип і концентрація використовуваних добавок, а також умови технологічної обробки безпосередньо впливають на потенційний профіль Extractables. Термічні навантаження, процеси стерилізації та тривалий контакт із лікарським засобом можуть змінювати поведінку матеріалів і, відповідно, їхню хімічну сумісність із продуктом.
З позицій дизайну процесу це означає, що вибір матеріалів має ґрунтуватися не лише на урахуванні фізико-механічних або бар’єрних характеристик, а й на прогнозованій хімічній взаємодії з лікарською формою в реальних умовах застосування.
Вторинне та третинне пакування (secondary та tertiary packaging)
Хоча вторинне та третинне пакування не контактує безпосередньо з лікарським засобом, воно може опосередковано впливати на загальний профіль ризиків. Клеї, фарби, друкарські покриття, барвники та адгезивні матеріали потенційно можуть бути джерелом летких або мігруючих сполук, особливо за умов тривалого зберігання, підвищеної температури або герметичного пакування.
З огляду на це сучасний дизайн пакування передбачає оцінку всієї пакувальної системи як єдиного цілого — від первинних компонентів до матеріалів для маркування та вторинних елементів. Потенційні джерела E&L у пакувальній системі узагальнено наведено на рисунку.
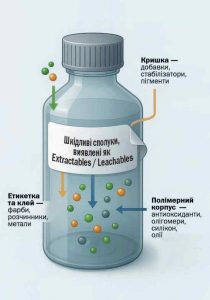
Рисунок. Джерела E&L у фармацевтичному пакуванні, які важливо враховувати в дизайні пакувальної системи та оцінці хімічної сумісності
Таким чином, E&L виступають інтегруючим елементом між вибором матеріалів, конструкцією пакувальної системи та подальшим аналітичним контролем. Усвідомлення E&L як параметра дизайну дозволяє знизити регуляторні та технологічні ризики та створює передумови для побудови обґрунтованої аналітичної стратегії на наступних етапах життєвого циклу лікарського засобу.
4. Аналітична стратегія: не метод, а система
У контексті ризик-орієнтованого дизайну пакування та матеріалів для технологічного виробництва аналітичний підхід до E&L не може бути обмежений вибором окремого методу або інструменту. Аналітична стратегія в E&L-дослідженнях формується як система взаємопов’язаних рішень, що безпосередньо випливає з характеристик контактуючих матеріалів, умов контакту та очікуваного профілю ризиків, визначених на етапі створення дизайну пакувальної системи або під час вибору матеріалів для технологічного виробництва.
Screening- та targeted-аналіз: різні задачі — різні підходи
Принциповим елементом побудови ефективної E&L-стратегії є чітке розмежування підходів screening та targeted, які вирішують різні аналітичні задачі і відповідають різним етапам оцінки ризиків.
Screening-аналіз призначений для широкого виявлення потенційних екстрагованих речовин (Extractables) у так званих worst-case умовах і є інструментом для проведення первинної ідентифікації ризиків. Його мета полягає у формуванні уявлення про хімічний «ландшафт» матеріалу включно з невідомими або частково охарактеризованими речовинами, а не у кількісній оцінці кожного компонента. Саме на цьому етапі аналітичні дослідження орієнтовані на отримання максимально інформативних даних (точної маси, ізотопного розподілу та структурної фрагментації), що дозволяє ідентифікувати як відомі, так і невідомі аналіти включно з продуктами взаємодії матеріалів пакування з компонентами лікарського засобу. Натомість дослідження Leachables здебільшого ґрунтуються на таргетному підході, спрямованому на надійне кількісне визначення та контроль заздалегідь ідентифікованих речовин у реальних умовах зберігання та застосування лікарського засобу. В цьому контексті ключового значення набувають селективність і специфічність аналітичних методів, а також урахування матричних ефектів, що є критично важливим для забезпечення стабільного та регуляторно обґрунтованого кількісного контролю.
5. Роль мас-спектрометричних підходів
З огляду на різноманіття потенційних джерел E&L жоден універсальний аналітичний інструмент не здатний охопити всі класи речовин. Саме тому сучасна E&L-стратегія передбачає комплементарне використання аналітичних підходів, кожен з яких вирішує окремий клас задач.
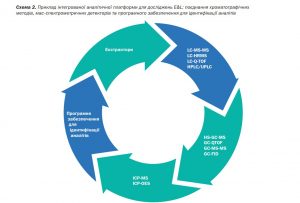
Приклад інтегрованого підходу до вибору аналітичних інструментів та програмного забезпечення для реалізації E&L-стратегії наведено на схемі 2.
Методи на основі газової хроматографії з мас-спектрометричним детектуванням є ключовими для роботи з леткими та низько-молекулярними органічними сполуками, тоді як рідинна хроматографія з мас-спектрометрією дозволяє аналізувати менш леткі, полярні або термолабільні компоненти, характерні для багатьох полімерних матеріалів і добавок. ICP-MS, своєю чергою, є незамінним інструментом для оцінки елементних домішок, пов’язаних із застосуванням як пакувальних матеріалів, так і матеріалів для технологічного виробництва.
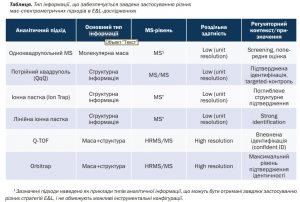
Як приклад, одноквадрупольні мас-спектрометри надають інформацію про молекулярну масу та можуть бути використані на етапі первинного screening-аналізу. Потрійні квадруполі та іонні пастки, завдяки застосуванню MS/MS
або MSn, дозволяють отримувати структурну інформацію, а також ними послуговуються для підтвердження ідентичності або таргетного контролю відомих речовин. Високороздільні мас-спектрометричні підходи (HRMS), зокрема Q-TOF та Orbitrap, поєднують точне визначення маси зі структурною інформацією та забезпечують найвищий рівень підтвердження ідентичності, що є критично важливим під час роботи з невідомими речовинами, продуктами взаємодії матеріалів пакування з лікарським засобом, а також із метою ухвалення складних регуляторних рішень.
Отже, вибір підходу low-resolution або high-resolution визначається не типом приладу як таким, а рівнем необхідної аналітичної впевненості та контекстом застосування результатів. Виходячи з цього, вибір аналітичного підходу залежить від природи очікуваних речовин і типу інформації, необхідної для ухвалення регуляторних рішень, а не конкретного виробника обладнання. Одним із ключових при цьому залишається досягнення балансу між аналітичною чутливістю та можливістю коректної інтерпретації отриманих даних. У рамках системного підходу до E&L вирішальним є не максимальне зниження межі виявлення, а отримання релевантної, інтерпретованої та регуляторно обґрунтованої інформації, інтегрованої в CCS протягом усього життєвого циклу продукту (таблиця).
Різний рівень аналітичної інформації, що використовують на етапах оцінки Extractables та контролю Leachables, неминуче впливає на підходи до валідації аналітичних методів. У межах сучасної ризик-орієнтованої парадигми валідація E&L-методів перестає бути формальним застосуванням класичних вимог і дедалі більше орієнтується на принцип fit-for-purpose, тобто відповідність методу поставленій аналітичній та регуляторній задачі.
Валідація для Extractables: фокусна ідентифікації
На етапі оцінки профілю Еxtractables аналітичні методи зазвичай застосовують для роботи з невідомими або частково охарактеризованими речовинами. У таких випадках класичні параметри валідації, зокрема точність або лінійність, не завжди можуть бути використані у повному обсязі. Натомість ключового значення набувають специфічність методу, здатність до надійної ідентифікації та інтерпретації аналітичних сигналів, а також відтворюваність якісної інформації.
У цьому контексті широко використовують напівкількісні підходи, внутрішні стандарти або модельні сполуки, що дозволяють здійснити регуляторно прийнятну оцінку ризиків навіть за відсутності повністю охарактеризованих стандартів для кожної виявленої речовини. Отже, валідація методів для Еxtractables спрямована насамперед на підтвердження придатності методу для ідентифікаційних цілей, а не на досягнення максимальної кількісної точності.
Валідація для Leachables: кількісний та матрично-орієнтований підхід
На відміну від Extractables, дослідження Leachables зазвичай виконують в умовах реальної матриці лікарського засобу. Вони мають на меті контроль заздалегідь ідентифікованих речовин. У цьому випадку валідація методів повинна забезпечувати стабільне та відтворюване кількісне визначення, що відповідає регуляторним вимогам.
Особливу роль відіграють підтвердження селективності та специфічності, а також оцінка матричних ефектів, які можуть суттєво впливати на точність і відтворюваність результатів. Саме ці аспекти визначають надійність контролю Leachables протягом усього терміну придатності продукту та його відповідність встановленим лімітам безпеки.
 Валідація як елемент життєвого циклу
Валідація як елемент життєвого циклу
У світлі вимог EU GMP Annex 1 та підходів, що формуються в межах ICH Q3E, валідацію E&L-методів розглядають не як одноразову подію, а як динамічний процес, інтегрований у життєвий цикл лікарського засобу та його пакування. Зміни у матеріалах, конструкції пакувальної системи або технологічних умовах можуть потребувати перегляду як аналітичної стратегії, так і параметрів валідації.
Сучасна валідація E&L-методів є логічним продовженням ризик-орієнтованого дизайну та аналітичної стратегії. Вона дозволяє узгодити рівень аналітичної деталізації з реальними регуляторними та токсикологічними потребами і трансформуватир езультати E&L-досліджень в обґрунтовані рішення з управління ризиками.
6. Вплив E&L на QC та лабораторну стратегію
Інтеграція E&L у дизайн пакування та аналітичну стратегію змінює роль лабораторій контролю якості, які дедалі частіше залучають до ризик-орієнтованого управління контамінацією протягом усього життєвого циклу лікарського засобу. Контроль Leachables виходить за межі рутинного аналізу і вимагає застосування стабільних, селективних та відтворюваних кількісних методів з урахуванням матричних ефектів і можливих змін під час зберігання продукту.
У цьому контексті вибір аналітичного обладнання набуває стратегічного характеру та визначається запланованим обсягом E&L-досліджень — від таргетного контролю до розширеної ідентифікації потенційних ризиків. Ключовим фактором стає неуніверсальність інструментів, а здатність лабораторії отримувати та інтерпретувати інформацію, релевантну для ухвалення регуляторних рішень.
У світлі підходів, які формуються в межах ICH Q3E, а також на підставі вимог EU GMP Annex 1 щодо впровадження CCS лабораторна стратегія має бути гнучкою та орієнтованою на довгострокову перспективу. Це передбачає готовність до адаптації аналітичних підходів у разі змін пакувальних матеріалів, конструкції контейнерно-закупорювальної системи або технологічних процесів, а також відповідний розвиток експертних компетенцій.
Зростання складності E&L-задач впливає не лише на технічне оснащення, але й на організаційні моделі роботи лабораторій. Поєднання внутрішніх ресурсів із залученням спеціалізованих лабораторій дедалі частіше розглядають як частину узгодженої стратегії управління ризиками. Зазначимо, що E&L впливають не лише на окремі аналітичні методи, але й назагальну архітектуру лабораторної діяльності, формуючи нові вимоги до QC та збереження безпеки продукту в умовах зростаючих регуляторних очікувань і технологічної складності.
E&L як стандарт майбутнього пакування
Розвиток матеріалів для пакування та посилення регуляторних вимог приводять до того, що E&L дедалі більше розглядають як невід’ємний елемент дизайну пакування та управління ризиками, а не як допоміжне аналітичне завдання. Підходи, що формуються в межах ICH Q3E, у поєднанні з вимогами EU GMP Annex 1 щодо впровадження CCS відображають перехід від реактивного контролю до проактивної, науково обґрунтованої моделі управління хімічною сумісністю. Це означає, що оцінку E&L необхідно інтегрувати в процес ухвалення рішень уже на етапі вибору пакувальних матеріалів і матеріалів для технологічного виробництва.
У цьому контексті E&L виконують роль зв’язувальної ланки між інноваціями в пакуванні, аналітичною стратегією та регуляторною відповідальністю. Очікується, що на майданчиках накшталт Interpack-2026 питання щодо нових матеріалів і ухвалення сталих рішень дедалі тісніше поєднуватимуться з оцінкою E&L як ключового чинника безпеки лікарського засобу.
Підсумовуючи, зазначимо, що системна інтеграція E&L у процес розробки, аналітичні та валідаційні підходи формує новий стандарт фармацевтичного пакування, орієнтований на досягнення балансу між інноваціями та захистом пацієнта.
Практичні аспекти інтеграції E&L у дизайн пакування, аналітичну та валідаційну стратегію також розглядають в межах професійних технічних матеріалів, зокрема у записах спеціалізованих вебінарів ISPE Ukraine, присвячених цій темі.
Ілюстрації згенеровані з допомогою ШІ або надані авторкою статті.