Автори: Валентин Могилюк (valentyn.mohylyuk@rsu.lv), Arturs Paulausks, Oskars Radzins, Liga Lauberte
Leading Research Group, Faculty of Pharmacy, Rīga Stradiņš University, Riga, Latvia
Ключові слова: таблетки; целюлоза мікрокристалічна; кальцію фосфат; діаграма Геккеля; міцність на стискання; профіль тиск — зміщення.
Анотація
Використання в процесі пресування мікрокристалічної целюлози (MКЦ) з пластичними властивостями та безводного кальцію фосфату (CaHPO4), що має крихкі властивості, є дуже популярним у фармацевтичній промисловості методом для досягнення бажаних структурно-механічних властивостей таблетованих форм. У цьому дослідженні випробувані суміші певних марок MКЦ і CaHPO4 в об’ємних пропорціях 100–0, 75–25, 50–50, 25–75 і 0–100 за постійної масової концентрації лубриканта натрію стеарилфумарату, а також застосований сучасний симулятор компактування (STYL'One Nano, KORSCH). Таблетки виготовляли за значень 100, 150, 250, 350, 450 і 500 МПа і оцінювали за профілем таблетування, профілем сили виштовхування, залежністю між складом та міцністю на стискання, залежністю між складом і пористістю, профілем тиск-зміщення та профілем пружного відновлення, а також відповідно до діаграми Геккеля в матриці та поза матрицею та середнім тиском плинності (Py). Цікаво, що композиція 25–75 поза матрицею продемонструвала двоступеневу діаграму Геккеля, її додатково дослідили за допомогою рентгенівської мікрокомп’ютерної томографії ( CT). Вивчивши результати CT, рівень крихкої деформації частинок CaHPO4 як функцію від тиску пресування кількісно визначали за допомогою співвідношення площі поверхні CaHPO4 до об’єму CaHPO4 (S/V). Для композиції 25–75 першу (до 150 МПа) і другу (вище 150 МПа) стадії діаграми Геккеля поза матрицею можна пояснити переважним впливом деформації MКЦ і CaHPO4 відповідно.
1. Вступ. Таблетки є одним із найефективніших шляхів виробництва фармацевтичних та нутрицевтичних продуктів. Змішування двох або більше компонентів у відповідних пропорціях дозволяє отримати таблетку з бажаними властивостями [1]. Структурно-механічні властивості таблеток мають особливе значення. Механічні властивості впливають на можливість і якість подальшої обробки, наприклад нанесення покриття і пакування, тоді як структурні — можуть впливати на біофармацевтичні властивості таблеток, наприклад на розчинення лікарського засобу. Крім того, під час розробки генеричних таблеток одними з найважливіших завдань є деформуляція складу оригінального препарату (з’ясування використаних компонентів), а також розуміння властивостей і поведінки допоміжних речовин у процесі виготовлення. Суміші речовин із пластичною та крихкою деформацією можуть позитивно вплинути на фізичну взаємодію під час компактування [2–4]. Серед доступних прикладів добре відома і дуже популярна у виробництві таблеток комбінація пластичної мікрокристалічної целюлози (МКЦ) і крихкого кальцію фосфату (CaHPO4) [4, 5]. Обидві допоміжні речовини представлені на ринку у вигляді різноманітних сортів від різних виробників. Сорти МКЦ відрізняються за розміром, формою, площею поверхні, кристалічністю та вмістом вологи, в той час як CaHPO4 може мати різну гранульовану форму (у вигляді агрегованих кристалів) [6–11]. Сорт і пропорції МКЦ і CaHPO4 можуть впливати на пресування, ме- ханічні властивості й пористість, а отже, на проникнення води, розпад і вивільнення лікарської речовини в таблетках [12–16]. Слід зазначити, що CaHPO4 практично не розчиняється у воді, але розчиняється в розведених кислотах [6]. Різні пропорції та сорти CaHPO4 з різними розмірами частинок можуть впливати на вивільнення лікарських засобів in vitro [17, 18]. Така рН-залежна розчинність може чинити вплив і на вивільнення препарату in vivo. Тому сорти та пропорції МКЦ і CaHPO4 необхідно ретельно підбирати, враховуючи як механічні, так і біофармацевтичні аспекти. Для кращого розуміння фундаментальних особливостей та взаємного впливу на структурно-механічні властивості було досліджено однокомпонентні та бінарні суміші МКЦ та CaHPO4. Додавання 25% (в/в) MКЦ до CaHPO4 призводило до збільшення здатності до пресування завдяки зростанню густини [2]. Зі збільшенням масової частки МКЦ спостерігали пряму залежність між середнім тиском плинності та пружним відновленням пресованого матеріалу. За всіх швидкостей прикладеної сили, зі збільшенням масової частки МКЦ, середній тиск плинності знижувався, тоді як пружне відновлення підвищувалося, що пояснюється домінуючою властивістю пластичної деформації МКЦ [5]. Бінарну суміш МКЦ і CaHPO4 досліджували для визначення взаємозв’язку між твердою фракцією, напругою під час стиснення та механічними властивостями. Виявлено, що пластична деформація зумовлена перколяційним кластероутворюванням [19]. Спираючись на фазу стиснення та час витримки (dwell time), оцінювали поріг перколяції CaHPO4 у суміші з МКЦ [20]. Належним чином обладнаний таблетпрес є технічною вимогою до проведення ретельного дослідження процесу таблетування та покращення розуміння фізичних процесів, а також визначення їхнього впливу на кінцеві структурно-механічні властивості таблеток. Останнім часом обладнання, таке як симулятори компактування з високотехнологічними датчиками і зручним для користувача програмним забезпеченням, стало більш доступним на ринку [21]. Це сприяє детальному вивченню таких добре відомих комбінацій допоміжних речовин, як МКЦ та CaHPO4. Метою цього дослідження було вивчення таблетування бінарних сумішей мікрокристалічної целюло- зи та двоосновного безводного кальцію фосфату (CEOLUSTM UF-711 та DI-CAFOS® A60 відповідно) у різних об’ємних співвідношеннях за різних зусиль пресування для ви значення та пояснення впливу складу суміші на структурно-механічні властивості.
2. Матеріали та методи
2.1. Матеріали
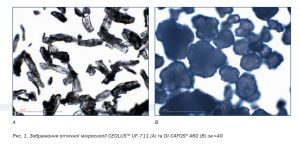
Порошок МКЦ (CEOLUSTM UF-711; Asahi Kasei; рис. 1А) та кальцію фосфат двоосновний безводний ( Ca H P O ; D I- C A FO S ® A 6 0; Budenheim KG; рис. 1B) використовували як основні компоненти для бінарних сумішей, тоді як кремнію діоксид (SYLOID® 244FP; Grace GmbH) і натрію стеарилфумарат (PRUV®; JRS Pharma) додавали до складу як глідант і лубрикант відповідно. Використання відповідних марок МКЦ, CaHPO4, кремнію діоксиду та натрію стеарилфумарату було зумовлене їхньою наявністю у лабораторії під час планування експерименту.
2.2. Мікроскопія
CEOLUSTM UF-711 та DI-CAFOS®A60 вивчали за допомогою оптичного мікроскопа (BA410E; Motic), оснащеного галогенною лампою потужністю 50 Вт і об’єктивами Motic EC-H Plan 4 /0,1, 10 /0,25 і 40 /0,65. Зображення робили ка-мерою MoticamProS5 Lite з про-грамним забезпеченням MoticImages Plus 3.0.
2.3. Приготування порошкових сумішей
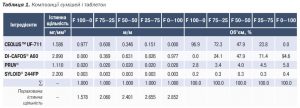
Об’ємне співвідношення розраховували, виходячи з істинної щільності компонентів; назви сумішей відображають об’ємне співвідношення MКЦ і CaHPO4. Зразки порошків (табл. 1) готували відповідно до тієї самої процедури. MКЦ, CaHPO4 та кремнію діоксид змішували протягом 10 хв у двоконусному блендері (DVC Developer; Comasa). Для забезпечення мікроскопічної однорідності отриману суміш обережно просіювали крізь сито з розміром отворів 1 мм і знову перемішували протягом 5 хв. На наступному етапі натрію стеарилфумарат просіювали крізь сито з розміром отворів 0,5 мм, додавали до преміксу і потім перемішували впродовж 2 хв. Отриману суміш просіювали крізь сито з розміром отворів 1 мм і знову перемішували протягом 2 хв.
2.4. Приготування таблеток
Таблеткові суміші пресували за допомогою плоских пуансонів діамеіаметром 11,28 мм до отримання цільової маси 500 мг із використанням симулятора компактуванняSTYL’One Nano.
Цикли пресування імітували роботу невеликого ротаційного преса з діаметром турелі 180 мм, діаметром валків попереднього пре-сування 44 мм, кутом між валками 65°, діаметром валків пресування 160 мм, кутом нахилу виштовхування 20° за імітованої швидкості таблетування 70 об/хв (максимальна для STYL’One Nano), зусиллям попереднього пресування 5 кН (50 МПа) і зусиллям спресування 10–50 кН (100–500 МПа). Подача порошку в матрицю здійснювалася автоматично через живильний башмак [22].
2.5. Вимірювання твердості таблеток та розрахунок міцності на стискання
Висоту (t), діаметр (d) і міцність на стискання (твердість або сила розламування, F) вимірювали (n = 10) за допомогою тестера для табле- ток (ST50 WTDH; SOTAX AG, Aesch, Швейцарія) одразу після пресування. Радіальному межу міцності (τ, МПа) розраховували за рівнянням [23]:
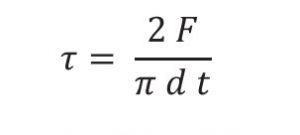
2.6. Обчислена істинна щільність
Обчислена істинна щільність рецептур таблеток отримана на основі щільності, визначеної за допомогою пікнометра ( t) МКЦ (1,586 г/см3) [7, 24], CaHPO (2,890 г/см3) [6], натрію стеарилфумарату (1,110 г/см3) [25], кремнію діоксиду (2,200 г/см3) [26] та їхніх сумішей із використанням адитивної методології і рівняння [27]:
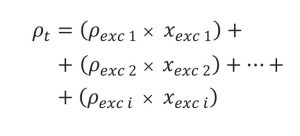
2.7. Обчислення видимої щільності, пористості та твердої фракції
Відносний об’єм та щільність таблеток визначали після виштовхування з матриці. Видиму щільність (ρ) таблеток розраховували як відношення маси таблетки (Wtab) до об’єму циліндра за рівнянням:
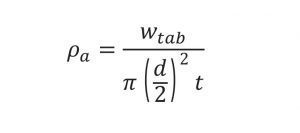
Тверду фракцію (SF) і пористість (ε) таблетки розраховували за рівняннями [28]:
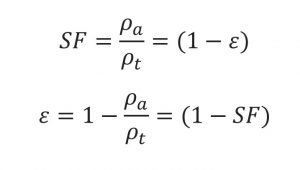
2.8. Побудова діаграми Геккеля Діаграму Геккеля в матриці — відносну щільність ln(1/ε) — визначали за допомогою програмного забезпечення Alix версії 20220711 (Medelpharm/Korsch) [29]. Показники відносної щільності та тиску ущільнення (P , МПа) розраховували відповідно до рівняння Геккеля [30]:
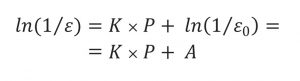
де K — нахил лінійної ділянки (постійна пропорційності) і ln(1/ε0) — постійна A, яка виражає ступінь ущільнення (за пористості ε0), що досягається за низького тиску через процес перегрупування до того, як відбудеться помітна кількість міжчастинкових зв’язків. Для діаграми Геккеля поза матрицею відносну щільність n(1/ε) визначали на основі об’єму виштовхнутої таблетки та розрахованої пористості (ε) для кожного тиску пресування (n = 10). Для всіх сумішей лінійна ділянка була обрана між 100 і 150 МПа, в той час як для F 25–75 і F 0–100 також була проаналізована лінійна ділянка між 250 і 450 МПа. Py розраховували, використовуючи рівняння [31]:
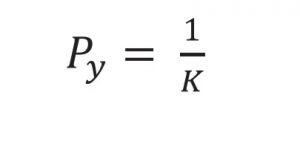
2.9. Еластичне відновлення Еластичне відновлення (ER ) розраховували як відсоток відновлення висоти таблетки на основі її висоти після виштовхування (hejected) і мінімальної висоти в матриці (hin-die) [29], використовуючи рівняння:
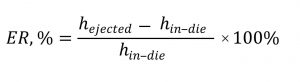
2.10. Рентгенівська мікрокомп’ютерна томографія ( CT) зразків таблеток Невеликий шматочок таблетки (приблизно 5 мм3) відламували і сканували за допомогою 3D мікрорентгенівського комп’ютерного томографа (CT Lab HX; Rigaku Corp.) за напруги 70 кВ, струму 50 мкА, S-фокусуванні і без фільтра. Налаштування сканування: 5 FOV, довга геометрія, режим сканування з високою роздільною здатністю та надвисока роздільна здатність зображення (час сканування — 68 хв). Скани таблетки експортували у вигляді DCM-файлів і обробляли за допомогою програмного забезпечення Dragonfly (Dragonfly, версія 2022.2.0.1409; Object Research Systems (ORS) Inc.). З цих сканів виділяли репрезентативний 3D-фрагмент внутрішнього об’єму зразка таблетки. При цьому циліндричний фрагмент 3D-зображення внутрішнього об’єму таблетки ізолювали від усього 3D-зображення. Потім зображення фрагменту розділили на три області (ROI): перша — це частинки CaHPO4 (через високу контрастність); друга — область без CaHPO4, яка складалася з МКЦ, інших допоміжних речовин і повітря; третя — вся область (перша і друга). Об’ємний відсоток частинок CaHPO4 і область, що не містить CaHPO4, розраховували відносно ROI усього простору. Площу поверхні частинок CaHPO4 визначали за допомогою алгоритму Лоренсена і нормалізовували для кожного зразка за допомогою поділу на об’єм маскувального циліндра. На основі використаного методу комп’ютерної томографії рентгенографічні проєкції об’єднували для побудови 2D-зрізів зразка таблетки з подальшою 3D- реконструкцією зразка. Кінцеві зображення складалися з вокселів із різними рівнями сірого, що відповідали різним значенням щільності [32]. Налаштування рівнів сірого може впливати на визначений об’єм CaHPO4, тому його використовували однаково для всіх оброблених зразків.
3. Результати та їх обговорення Деформацію під час таблетування можна безсумнівно вважати об’ємною деформацією. Об’ємний вміст окремих компонентів у бінарній суміші та їхні механічні властивості зумовлюють деформацію цих сумішей і впливають на механічні властивості таблеток. У процесі компактування об’єм компонентів таблеток наближається до об’єму за істинної щільності, тому після компактування об’єм компонентів відносно близький до об’єму за істинної щільності. Вплив об’ємного співвідношення компонентів (розрахованого на основі пікнометричної щільності окремих компонентів) на деформацію під час таблетування та механічні властивості таблеток у фокусі нашого інтересу, тому різні пропорції МКЦ та CaHPO4 були використовували у рецептурах (табл. 1). Збільшення фракції CEOLUSTM UF-711 зменшувало сипкість порошкової суміші. Отже, до кожної композиції додавали фіксовану масову концентрацію гліданта. У той самий час масова концентрація лубриканта натрію стеарилфумарату була постійною для всіх композицій. Це призвело до збільшення об’ємних часток гліданта та лубриканта, а також до збільшення пропорцій CaHPO4 високої істинної щільності. Кількість лубриканта була обґрунтована профілем сили виштовхування таблетки (рис. 2B): за тиску стиснення до 300 МПа тиск виштовхування не перевищував 3 МПа [33]. Межа міцності на стискання формуляції МКЦ (F 100–0) зростала з підвищенням тиску пресування в діапазоні 100–450 МПа, хоча зростання тиску пресування з 450 до 500 МПа не призводило до подальшого збільшення міцності таблеток (рис. 2А).
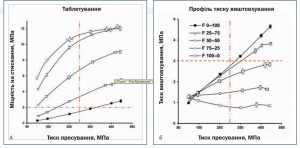
Рис. 2. Межа міцності на стискання (А) і тиск виштовхування таблеток (Б) як функції від тиску пресування
У той самий час суміш CaHPO4 (F 0–100) продемонструвала майже лінійне зростання міцності на стискання таблеток від 100 до 500 МПа. Для кожного значення тиску ущільнення межа міцності на стискання таблеток із МКЦ була значно вищою, ніж для таблеток із CaHPO4. Зни- ження вмісту МКЦ у рецептурі супроводжувалося зменшенням міцності таблеток (рис. 2А), що узгоджується з доступними даними [5]. Виходячи з припущення, що міцність/твердість таблетки відображає зв’язок, який виникає під час таблетування [1], можна зро- бити висновок, що когезія МКЦ є вищою, ніж адгезія МКЦ — CaHPO4, яка, своєю чергою, вища, ніж когезія CaHPO4. Тим не менш міжмолекулярні сили можуть бути змінені внаслідок застосування лубриканта [34–36]. Враховуючи вищевикладене, не слід ігнорувати можливий вплив лубриканта на ефективність адгезії. DI-CAFOS® A60 має меншу видиму питому поверхню порівняно з такою CEOLUSTM UF-711 (рис. 1), що супроводжується меншим питомим об’ємом DI-CAFOS® A60 через його вищу істинну щільність (2,890 проти 1,586 г/см3 відповідно; табл. 1). Це робить її більш чутливою до підвищення вмісту лубриканта. Іншими словами, на додаток до порівняно нижчої когезії CaHPO4 за меншої питомої поверхні вплив тієї самої кількості лубриканта на зниження міцності на стискання є більш вираженим. Однак навіть у разі підвищення об’ємної частки лубриканта збільшення об’ємної частки CaHPO4 і сили ущільнення призводить до зростання сили виштовхування (табл. 1 і рис. 2B). Зазвичай тиск 300–500 МПа є максимальним значенням для таблетування лікарських засобів [37]. Для успішного формування 300 МПа вважають максимально допустимим тиском пресування і 2 МПа — мінімально допустимою межею міцності таблеток на стискання, що відповідають фармакопейним вимогам [33]. Вищезазначені максимально допустимий тиск пресування та мінімально допустима межа міцності на стискання зображені вертикальною та горизонтальною червоними лініями відповідно (рис. 2А). З практичної точки зору, в умовах імітації роботи ротаційного преса з частотою обертання 70 об/хв рецептура F 0–100 CaHPO4 може забезпечити бажану міцність на стискання таблеток лише за тиску стиснення 350 МПа, тоді як суміш F 25–75 демонструє таку міцність вже за тиску понад 150 МПа. У той же час F 50–50, F 75–25 і F 100–0 могли забезпечити бажану міцність таблеток на стискання навіть за відносно низького тиску стиснення 100 МПа (рис. 2А). Під час пресування зменшення пористості збільшує площу контакту, зчеплення та підвищує міцність на стискання. Однак здатність інгредієнтів та їхніх сумішей зменшувати пористість залежно від тиску є різною і може бути охарактеризована середнім зусиллям плинності. Цікаво, що профілі співвідношення компонентів і міцності на стискання, отримані за всіх значень тиску пресування для об’єму МКЦ від 25 до 75%, показали майже лінійну залежність (рис. 3А), де міцність на стискання зростала у міру підвищення вмісту МКЦ і тиску пресування. У тому самому діапазоні об’єму МКЦ профілі співвідношення пористості також демонструють майже лінійну залежність (рис. 3В), де пористість зменшується разом зі зниженням вмісту МКЦ і зростанням тиску пресування. Нелінійну залежність в діапазоні об’єму МКЦ від 0 до 25% і від 75 до 100% можна пояснити порогами перколяції CaHPO4 і МКЦ відповідно (рис. 3).
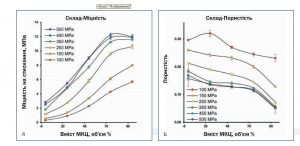
Рис. 3. Межа міцності на стискання (А) та пористість (В) як функція вмісту МКЦ (для наочності червоним кольоромвиділено смуги похибок за 500 МПа)
Залежність пористості від вмісту МКЦ (рис. 3B) можна використати для пояснення того, як міцність на стискання таблетки (рис. A) контролюється щільністю. Це пов’язано з тим, що за певного значення тиску пресування порошок більше не може бути ущільнений. На відміну від діапазону тиску пресування 100–350 МПа, за 350–500 МПа відносно невелика зміна пористості призвела до незначної зміни міцності на стискання (рис. 3В порівняно з рис. 3А). Профілі тиску — зміщення у матриці відображають різницю в істинній щільності різних формуляцій. За однакового заданого тиску пресування до рецептур із високим вмістом CaHPO4 відстань між пуансонами має бути меншою, що результує у тонші таблетки через вищу істинну щільність CaHPO4 порівняно з МКЦ (рис. 4А). Окрім того, у разі зниження вмісту МКЦ і підвищення — CaHPO4 середній тиск плинності (Py) в матриці поступово зростав — від 94 МПа (F 100–0) до 350 МПа (F 0–100) (рис. 4Б). Оскільки середній тиск плинності в матриці можна використовувати як показник пластичності матеріалу [38], пластичність сумішей очікувано зростала від CaHPO4 до МКЦ формуляції (від F 0–100 до F 100–0 відповідно). Беручи до уваги виміряні значення для сумішей із комбінаціями МКЦ — CaHPO4, середній тиск їхньої плинності в матриці не може бути передбачений за допомогою адитивної методології (наприклад, як для розрахованої істинної щільності) на основі тиску плинності в матриці F 0–100 і F 100–0. Як і очікувалося, після виштовхування з матриці підвищення вмісту МКЦ підвищувало значення еластичного відновлення (рис. 4В).
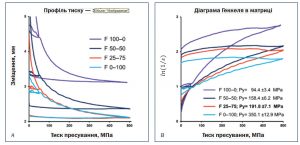
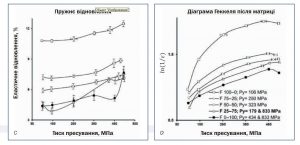
Рис. 4. Профіль залежності тиску від зміщення в матриці (A), діаграма Геккеля в матриці (B), еластичне відновлення (C), діаграма Геккеля після виштовхування з матриці (D)
Суміші F 100–0, F 75–25 і F 50–50 продемонстрували збільшення значень еластичного відновлення зі зростанням тиску пресування. Профіль еластичного відновлення для F 0–100 мав відносно великі стандартні відхилення, тоді як F 25–75 — порівняно складну форму, а еластичне відновлення F 25–75 і F 0–100 також збільшувалося зі зростанням тиску пресування. Різниця між щільністю таблеток у матриці та після виходу з матриці залежить від еластичного відновлення. Відповідно до діаграми Геккеля середній тиск плинності (Py) в матриці для МКЦ (F 100–0) був найнижчим і становив 106 МПа, тоді як середній тиск плинності (Py) в матриці для CaHPO4 (F 0–100) був найвищим і становив 434 МПа. Цікаво, що суміш F 25–75 (Py179 МПа) не відповідала послідовності підвищення середнього тиску плинності (Py) після виходу з матриці зі зростанням вмісту CaHPO4. Однак кут нахилу першої частини кривої був близьким до такого для МКЦ (F 100–0), тоді як інша частина кривої була паралельною до кривої для CaHPO4 (F 0–100). Ця подібність підтверджується однаковим значенням Py (833 МПа) для порівняного діапазону тиску пресування 250– 450 МПа (рис. 4Г). Можна припустити, що ущільнення F 25–75 було зумовлене МКЦ (незважаючи на низький вміст МКЦ) у діапазоні тиску пресування 100–150 МПа і також вмістом CaHPO4 (рис. 5) в діапазоні тиску пресування 150– 500 МПа.
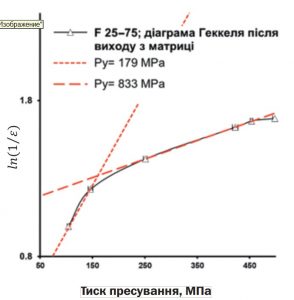
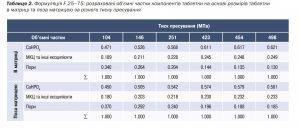
Рис. 5. Формуляція F 25 – 75: діаграма Геккеля післявиходу з матриці
Формуляцію F 25–75 дослідили більш ретельно. Після виштовхування таблетки зниження об’ємного вмісту компонентів у видимому об’ємі таблетки зумовлене еластичним відновленням. За значень 100, 150, 250 МПа і навіть вищих показників тиску пресування розрахована об’ємна частка CaHPO4 становила 0,471, 0,526 і 0,568 і вище в матриці, а також 0,450, 0,505 і 0,542 і вище поза неї відповідно (рис. 6A; табл. 2).
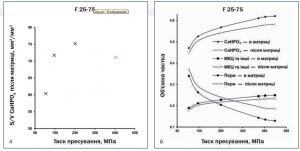
Рис. 6. Формуляція F 25–75: розраховані об’ємні частки компонентів таблетки за різного тиску пресування на основірозмірів таблетки в матриці та поза матрицею (A); співвідношення поверхня/об’єм для CaHPO4 після виходу з матриціна основі вимірювань методомCT для таблеток, виготовлених за різного тиску пресування (B)
Розрахована об’ємна частка CaHPO4 збільшилася разом із підвищенням тиску пресування, таку саму тенденцію спостерігали для об’ємної частки CaHPO4, виміряної µCT (рис. 7A; 7B).

Рис. 7. Формуляція F 25–75:CT-сканування частини таблетки під впливом тиску 104 МПа (А) і 454 МПа (В). Відео тривимірної реконструкції F 25–75 на основі вимірювань методом µCT доступні в Додаткових матеріалах
Незважаючи на МКЦ-подібну діаграму Геккеля поза матрицею в діапазоні тиску ущільнення 100–150 МПа, результати дослідження з використанням CT показали збільшення співвідношення площі поверхні CaHPO4 до об’єму CaHPO4 (S/V) (100 проти 150 МПа; рис. 6B), що свідчить про руйнування частинок CaHPO4 при підвищенні тиску пресування від 100 до 150 МПа. Зростання тиску пресування до 250 МПа відповідно збільшило співвідношення CaHPO4 S/V, що свідчить про подальше руйнування/крихку деформацію частинок CaHPO4 (рис. 6B). Однак попри збільшення об’ємної частки CaHPO4 і візуальне зменшення розміру частинок CaHPO4 (рис. 7, Додаткові матеріали), значення співвідношення S/V для CaHPO4 за 450 МПа неочікувано виявилося занадто низьким (рис. 6B). Автори припускають, що співвідношення S/V CaHPO4 за 450 МПа є не відповідає реальності та зумовлене обмеженнями налаштування використаного методу CT.
Висновки
Було досліджено суміші MКЦ — CaHPO4 з об’ємним вмістом 100– 0, 75–25, 50–50, 25–75 і 0–100, а також відповідними об’ємними частками лубриканта 2,8, 3,4, 4,0, 4,5 і 5,0. Одночасне збільшення як частки об’єму лубриканта, так і частки об’єму CaHPO4 було підтверджено профілем сили виштовхування. Зі зменшенням об’ємної частки МКЦ спостерігали зниження міцності таблетки на стискання, що частково можна пояснити збільшенням об’ємної частки лубриканта. Для всіх формуляцій у разі підвищення тиску пресування було виявлено зменшення пористості та підвищення міцності на стискання. У діапазоні об’ємної частки МКЦ від 25 до 75% збільшення міцності на стискання і зменшення частки пористості відбувалося лінійним чином. Суміш F 25–75 продемонструвала складний пружний профіль відновлення та двоступеневу діаграму Геккеля поза матрицею. Перший етап можна пояснити вмістом МКЦ, другий — деформацією CaHPO4. Збільшення крихкої деформації CaHPO4 в суміші F 25–75 в діапазоні тиску пресування від 100 до 250 МПа додатково підтверджено методом μCT.
У цьому дослідженні було показано, що симулятор компактування є потужним інструментом для глибокого та детального дослідження змінних складу, процесу пресування та їхнього впливу на властивості отриманих таблеток. Дослідження комбінацій різних марок МКЦ і CaHPO4 може бути потенційним напрямом подальшої роботи.
Цитувати як: Mohylyuk, V., et al., The Effect of Microcrystalline Cellulose–CaHPO4 Mixtures in Different Volume Ratios on the Compaction and Structural– Mechanical Properties of Tablets. Pharmaceutics, 2024. 16(3), DOI: 10.3390/pharmaceutics16030362.
Додаткові матеріали та перелік використаних джерел за посиланням: https://www.mdpi.com/1999- 4923/16/3/362