Главная цель деятельности предприятий фармацевтической отрасли заключается в разработке и производстве высококачественных лекарств, которые улучшают здоровье и повышают благополучие людей во всем мире. К сожалению, из-за своих размеров и специфики рынок лекарственных препаратов подвержен
постоянному появлению контрафактной продукции. Фальсификаты представляют угрозу не только здоровью потребителей, но и интересам производителей оригинальной продукции, которые теряют доходы и средства для дальнейших исследований и разработки новых препаратов, а также могут столкнуться с репутационными рисками.
Глобальным ответом на проблемы обращения контрафактной продукции является сериализация, а на некоторых рынках – агрегация. Эти системы позволяют отслеживать всю цепочку движения лекарственных средств ‒ от производителя до конечного потребителя. Нормативные требования в области сериализации и агрегации вменяют производителям в обязанность маркировать лекарства уникальными кодами и передавать эти данные в центральную информационную систему (национальный центр регулирования), где хранятся все уникальные коды для каждой пачки лекарств. При выполнении любой операции в процессе движения лекарственных средств к потребителю коды считываются и сверяются онлайн с центральной системой, которая при любом нарушении или подозрении на подделку выдает сигнал тревоги.
Как обеспечить соблюдение нормативных требований без снижения эффективности производства?
Перед производством каждой партии лекарств все параметры сериализации (такие как уникальный 2D-код, срок годности, идентификатор партии и др.) должны быть установлены на P&V-машинах. Во время этого процесса можно столкнуться со следующими рисками и проблемами:
• Снижение производительности и наглядности процессов. Внедрение решения для сериализации и агрегации влияет на эффективность производства. Неадекватные решения могут привести к большому количеству ненужных простоев, что негативно влияет на объем производства. Кроме того, неоптимальные решения часто не дают достаточной информации о процессах, что затрудняет выявление и использование потенциала для оптимизации.
• Ошибки и отклонения. Ошибки в процессе сериализации могут оказать существенное влияние на
операционную деятельность предприятия и обусловить значительные затраты (так, например, неправильно напечатанные коды могут привести к отзыву с рынка целых партий) – этот риск особенно актуален для частичных и непроверенных решений.
• Регуляторные риски. Используемое решение должно соответствовать нормативным требованиям, предъявляемым как к процессам сериализации и агрегации для различных рынков, так и к фармацевтическим программным и аппаратным решениям. Ошибки при выполнении этих требований могут привести к серьезным последствиям.
• Адаптация к требованиям конкретной страны. Национальные требования, предъявляемые к
процессам сериализации и агрегации, могут различаться, поэтому решение должно быть гибким, чтобы учесть все особенности местного рынка.
Ответом на все эти риски и проблемы является MePIS GenCode – современное решение «под ключ» для процессов сериализации и агрегации.
MePIS GenCode – решение для автоматической и ручной сериализации и агрегации
MePIS GenCode – это комплексное решение, которое отвечает всем нормативным требованиям и доказало свою эффективность на производстве в компаниях разных стран (в Европейском Союзе, России,
Украине).
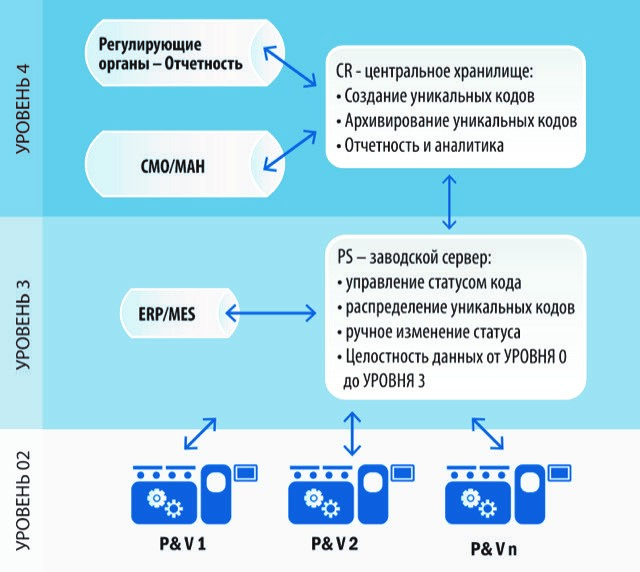
Система состоит из программного обеспечения L3 & L4 и программноаппаратных компонентов L0 – L2 (от производителя Inel) и легко интегрируется в существующую IT-среду, а также с MAH/CMO.
Существует три варианта MePIS GenCode для процессов сериализации и агрегации:
• Базовый – для производственных сред с ручной упаковкой.
• Стандартный – для средних производственных сред с комбинацией ручной и автоматической упаковки.
• Премиум – для крупномасштабных производственных сред с автоматической упаковкой.
Система MePIS GenCode соответствует требованиям, предъявляемым к процессам сериализации и агрегации, таким как Руководство ЕС 2016/161 и Постановление Правительства РФ № 1556, а также всем другим требованиям, регулирующим деятельность фармацевтической отрасли.
Основные преимущества системы MePIS GenCode

• Достижение полного соответствия нормативным требованиям в области сериализации и агрегации. Обеспечивает соблюдение требований по сериализации и агрегации на внутреннем и международном рынках.
• Обеспечение полного соответствия нормативам и GMP. Гарантирует соответствие системы сериализации нормативным требованиям для компьютеризированных систем в фармацевтической промышленности, описанным в GAMP5, Приложении 11 ЕС, 21 CFR Part 11 (включая контрольный журнал, электронные подписи и др.).
• Реализация оптимального решения для сериализации. Решение с большими функциональными возможностями, удобное в использовании и с разумной общей стоимостью владения.
• Полный контроль над процессами сериализации и агрегации. Полный обзор процессов сериализации и агрегации с помощью централизованного управления параметрами станка и процедурами, относящимися к процессу сериализации. Получение мгновенных автоматических уведомлений о событиях и необходимых действиях для всех заинтересованных сторон.
• Максимизация производительности. Отсутствие ошибок, задержек и отклонений в процессе сериализации и связанных с этим расходов благодаря наличию пошаговых инструкций для ключевых действующих лиц.
• Обеспечение целостности данных. Централизованное отслеживание и документирование всех изменений и действий в процессах сериализации и агрегации для обеспечения точности и согласованности данных в течение всего их жизненного цикла (отчеты, контрольные журналы и т. д.).
• Гибкие возможности подключений. Решение, которое легко интегрируется в существующую IT-инфраструктуру – с интерфейсами для уровней сериализации L2 – L3 – L4 и других IT-систем (ERP, WMS, MAH/CMO).
«Система MePIS GenCode может быть поставлена как готовое комплексное решение, которое включает в себя все необходимое: от разработки спецификации процесса, интеграции в упаковочные линии и тестирования до подготовки документации, передачи отчетности в центры регулирования и постоянной поддержки работы системы».