Г.А. Кордеро, Уповноважена особа, відповідальна за фармаконагляд, начальник відділу фармаконагляду, АТ «Фармак», Україна
М.І. Борщевська, Керівник департаменту з біотехнологій, АТ «Фармак», Україна
Г.І. Борщевський, Начальник лабораторії розробки технологій препаратів, АТ «Фармак», Україна
Застосування будь-якого лікарського засобу (ЛЗ) пов'язано з певними ризиками.
«Чи варто витрачати багато зусиль там, де можна обійтися малими засобами? Якщо ваше рішення виходить з нормативної вимоги, якщо ви в ньому впевнені – тоді не варто. Тут оцінка ризиків не потрібна. Але якщо ви перебуваєте в складній ситуації, то вам необхідно розуміти можливі загрози та їхні наслідки, визначати заздалегідь, яким чином діяти за того чи іншого розвитку подій, бути готовими до всього. Управління ризиками покращує передбачуваність і визначеність. Це чесно здобуте відчуття впевненості. Це, безумовно, підхід, що забезпечує достатній захист пацієнта, який, своєю чергою, не заважає отриманню прибутку і не уповільнює розвиток підприємства» (1).
Покладаючись на спонтанні повідомлення, представники уповноважених регуляторних органів можуть приймати такі екстрені регуляторні рішення, як відкликання препарату з ринку, відстрочка або відмова від його маркетування. Однак прийняття тільки радикальних рішень може стати причиною зменшення користі фармакотерапії для цільової популяції,
особливо без урахування наявності альтернатив на фармацевтичному ринку. Такого роду рішення можливі тільки в тому випадку, якщо співвідношення користь / ризик ЛЗ є неприйнятним або ризики виходять з-під контролю і стають некерованими. Очевидним є той факт, що попередження виникнення несприятливих наслідків фармакотерапії є більш доцільним, ніж вжиття заходів щодо їхнього усунення. Тому при здійсненні фармаконагляду відбулося зміщення акцентів у бік управління ризиками.
Складовою системи фармаконагляду є система управління ризиками.
Ризик – це вірогідність виникнення несприятливої ситуації або невдалий результат будь-якого процесу. Термін «ризик» не завжди, але зазвичай свідчить про щось негативне.
Про вміння професійно управляти ризиками, їхній сенс та цілі розказано в статті Групи «Віалек» (@ 2020 ГК «Виалек»)
Щодо ЛЗ поняття «ризик» ототожнюють із поняттям «побічна реакція». Управляти необхідно так званими важливими ризиками, тобто тими, які впливають на співвідношення користь / ризик ЛЗ, збільшуючи компоненту ризику в цьому співвідношенні.
Такими ризиками можуть бути ідентифіковані, для яких існують адекватні докази асоціації несприятливого наслідку із застосуванням певного препарату, а також потенційні, тобто несприятливі наслідки, при яких існує підозра чи гіпотеза щодо його зв'язку з певним ЛЗ, але чітка асоціація не підтверджена.
До важливих ризиків також належить і відсутність інформації. Якщо не управляти ризиками, пов'язаними із застосуванням ЛЗ, це може призвести до кризи, яка позначиться на стані здоров'я населення, на виробниках препаратів і на представниках регуляторних органів.
Отже, управління ризиками є єдиним способом вирішення проблеми після ідентифікації важливого ризику. Новий підхід до управління ризиками представлений в модулі V GVP «Система управління ризиками» (Risk management system), згідно з яким основною метою управління ризиками є досягнення максимально можливої переваги користі від застосування ЛЗ над ризиком для окремо взятого пацієнта цільової групи (2).
Система управління ризиками – це вид діяльності з фармаконагляду, спрямований на ідентифікацію, характеристику, запобігання або мінімізацію ризиків, пов'язаних із застосуванням ЛЗ, включаючи оцінку ефективності цих заходів.
Існує три стадії управління ризиками:
• характеристика повного профілю безпеки ЛЗ;
• планування діяльності з фармаконагляду для визначення характеру існуючих та ідентифікації нових ризиків, а також поповнення знань про профіль безпеки ЛЗ;
• планування та впровадження заходів з мінімізації і зниження ризиків, а також оцінка їхньої дієвості.
До рутинних заходів з мінімізації ризиків належать: маркування, зміст листка-вкладиша, короткої характеристики препарату, обмеження кількості готових лікарських форм в упаковці, відповідний правовий статус ЛЗ.
Додаткових заходів з метою мінімізації ризиків слід вживати тільки в разі потреби. Вони повинні бути обѓрунтованими, а також розробленими кваліфікованими фахівцями. Будь-які додаткові матеріали мають бути чітко орієнтованими на цілі мінімізації ризиків і не поєднуватися з рекламними матеріалами для проведення маркетингових кампаній.
Життєвий цикл ЛЗ – надзвичайно складний і тривалий процес. Достатньо сказати, що з декількох тисяч синтезованих речовин, з яких 250 вивчають на досліджуваних тваринах, п’ять допускають до клінічних досліджень і тільки одна речовина стає повноцінним ЛЗ. При цьому в клінічних дослідженнях беруть участь тисячі пацієнтів. Тривалість створення нового оригінального ЛЗ збільшилася в середньому з 8 до 15 років. Відповідно зростають і витрати на розробку ЛЗ, які в середині 90-х років минулого століття становили USD 300 – 500 млн (3).
Життєвий цикл ЛЗ складається з таких етапів:
1. Фармацевтична розробка (Q8 Pharmaceutical Development)
2. Доклінічні дослідження (Good Laboratory Practice)
3. Стандартизація (є однією з основних гарантій високої якості ЛЗ при серійному виробництві) (Good Storage Practice – GSP)
4. Клінічні дослідження (Good Clinical Practice – GCP)
5. Реєстрація
6. Виробництво (Good Manufacturing Practice – GMP)
7. Зберігання та логістика (Good Distribution Practice – GDP)
8. Реалізація споживачу (Good Pharmacy Practice – GPP (3 – 19).
Стандарти GXP забезпечують якість лікарського засобу на всіх етапах його життєвого циклу та безперервно оцінюють співвідношення користь / ризик (рис. 1).
 Ефективність препарату – це його здатність проявляти ефект (наприклад, знижувати артеріальний тиск). Ефективність ЛЗ може бути точно визначена тільки в ідеальних умовах (тобто у разі відбору пацієнтів згідно з належними критеріями і суворого дотримання режиму дозування препарату). Отже, ефективність ЛЗ визначають під керівництвом експертів у групі пацієнтів, у яких найімовірніше можна очікувати відповідної реакції на ліки (наприклад, в контрольованих клінічних випробуваннях).
Ефективність препарату – це його здатність проявляти ефект (наприклад, знижувати артеріальний тиск). Ефективність ЛЗ може бути точно визначена тільки в ідеальних умовах (тобто у разі відбору пацієнтів згідно з належними критеріями і суворого дотримання режиму дозування препарату). Отже, ефективність ЛЗ визначають під керівництвом експертів у групі пацієнтів, у яких найімовірніше можна очікувати відповідної реакції на ліки (наприклад, в контрольованих клінічних випробуваннях).
Результативність відрізняється від ефективності тим, що вона враховує, наскільки ефективний препарат в реальних умовах. Часто ЛЗ, який був ефективним в клінічних випробуваннях, виявляється малоефективним під час використання в медичній практиці. Наприклад, препарат може проявляти високу ефективність у зниженні артеріального тиску, але мати при цьому низьку результативність, оскільки під час його застосування виникає стільки побічних дій, що це може призвести до припинення пацієнтами прийому ЛЗ. Результативність препарату також може бути нижчою, ніж ефективність, якщо лікарі через необачність неправильно його призначають (наприклад, фібринолітичний препарат використовують у пацієнта з передбачуваним ризиком розвитку ішемічного інсульту, в якого за даними КТ не було виявлено внутрішньомозкового крововиливу). Отже, в такому випадку результативність є нижчою за ефективність.
ЯКІСТЬ ЛІКІВ – сукупність характеристик фармацевтичної продукції, які надають їй здатність задовольняти встановлені й передбачувані стандартами потреби (ISO 8402:1994). ЛЗ мають передусім проявляти лікувальну дію й бути безпечними. ВООЗ при розробленні національної медичної стратегії визначає, що ЛЗ повинні бути якісними, безпечними та
ефективними. У цьому випадку під терміном «якість» розуміють відповідність ЛЗ вимогам специфікацій якості, які чітко встановлюють відповідні норми та методи випробувань.
Вимоги до безпеки ЛЗ:
1. Відповідати вимогам Державної фармакопеї України та фармакопеям, що визнані чинними в Україні.
2. Мати оптимальну лікарську форму.
3. Містити тільки безпечні хімічно та фармакологічно сумісні активні компоненти і допоміжні речовини.
4. Мати безпечну тароупакувальну систему (інертність матеріалів, герметичність та функціональність), що забезпечує стабільність готового ЛЗ в ході визначеного терміну придатності за регламентованих умов.
5. Забезпечувати необхідними даними про безпеку готового ЛЗ, зазначеними в інструкціях для медичного застосуванням та на упаковках.
6. Зберігати стабільність упродовж терміну придатності.
7. Застосовувати лише за медичними показаннями з урахуванням даних оновленого профілю безпеки ЛЗ.
8. Зберігатись в умовах, які забезпечують відповідність фізико-хімічних і фармакологічних властивостей.
Сучасна методологія фармацевтичної розробки ЛЗ найповніше викладена в статті (20). Ми акцентуємо увагу на деяких критичних моментах в процесі розробки ЛЗ, які впливають на їхню ефективність та безпеку.
Взаємозв’язок оптичної ізомерії та фармакологічної активності ЛЗ
Відомі приклади використання в терапевтичній практиці рацематів, коли один зі стереоізомерів лікарської речовини проявляв значний токсичний ефект, що призводило до трагічних випадків. Наприклад, лівообертальний талідомідар – потужний транквілізатор, а наявні в суміші в рівних кількостях правообертальні ізомери мають тератогенну дію, що
спричиняє каліцтва у новонароджених.
У деяких випадках кількісні відмінності у біологічній активності двох енантіомерів одного і того самого з'єднання виражені значною мірою. Наприклад, дія D-ізомерів ізопротеренолаpу (препарат, який застосовують при легких нападах бронхіальної астми) як брондилататора в 50 – 70 разів сильніша, ніж L-ізомеру (Ленинджер А. і співавт., 1993).
Розпізнати стереоізомери речовини, що вводять в організм, можна на різних стадіях: при зв'язуванні з ферментами і рецепторами, при транспортуванні через мембрани, в процесі поглинання в клітинах і розподілу між тканинами.
Фізико-хімічні властивості АФІ та допоміжних компонентів та їхні технологічні параметри
Одне з основних завдань фармацевтичної розробки полягає в управлінні технологічним процесом і як наслідок – дотриманні стабільності продукту впродовж усього терміну зберігання.
 Фізико-хімічні властивості АФІ та допоміжних речовин впливають на визначення технологічних параметрів процесу (утворення домішок, розчинність, стійкість речовини до окиснення, сонячного світла, стабільність за різних температур тощо). Крім того, на якість готового продукту можуть впливати вибір обладнання для проведення оптимального технологічного процесу, матеріал і розмір фільтра (сорбція), коефіцієнт заповнення реактора та ін. (21).
Фізико-хімічні властивості АФІ та допоміжних речовин впливають на визначення технологічних параметрів процесу (утворення домішок, розчинність, стійкість речовини до окиснення, сонячного світла, стабільність за різних температур тощо). Крім того, на якість готового продукту можуть впливати вибір обладнання для проведення оптимального технологічного процесу, матеріал і розмір фільтра (сорбція), коефіцієнт заповнення реактора та ін. (21).
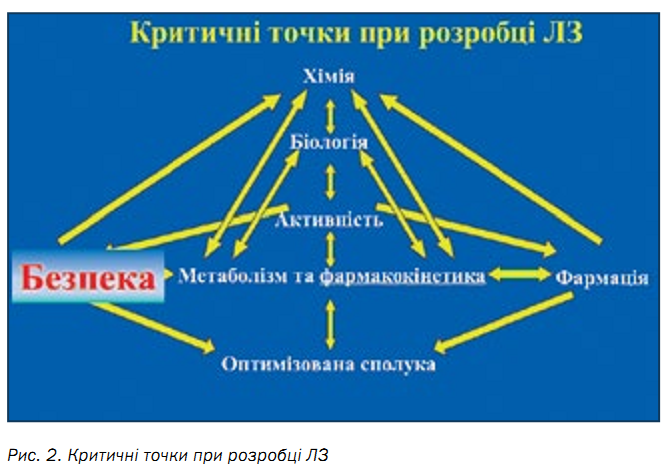
Критичні параметри процесу зручно характеризувати за допомогою методів фізики поверхні, оскільки це завжди пряме вимірювання. Зазвичай це сукупність технологічних параметрів (температура, тиск, швидкість перемішування, порядок внесення компонентів), дослідження теплообмінних процесів, хімічного складу та розташування атомів на
поверхні твердих тіл, а також теоретичне і експериментальне вивчення їхніх механічних, електронних і хімічних властивостей (рис. 2). Технологічний процес може бути поліпшений, якщо повністю вивчити поверхню (22).
До фізичних властивостей, що визначають якість готового продукту, належать:
• гранулометричний склад (розмір часток) – дуже важливий параметр, що визначає властивості вхідної сировини, проміжного і кінцевого продуктів (для твердих ЛЗ);
• реологічні властивості – надзвичайно важливі для розуміння зв'язку між технологією виробництва, експлуатаційними характеристиками і структурою матеріалів;
• калориметрія – сукупність методів вимірювання кількості теплоти, що виділяється або поглинається в процесі виробництва;
• дзета-потенціал – визначальний параметр для оцінки стабільності широкого кола дисперсних систем;
• визначення критичних параметрів процесу необхідне для масштабування та управління процесом, вивчення стабільності і складу препарату порівняння, поліморфізму, проведення вхідного контролю речовин та вибору первинної упаковки (23).
Взаємозв’язок кристалічної структури субстанції речовини, фармакокінетики та ефективності ЛЗ
Поліморфні зміни лікарських речовин можуть бути причиною швидкої інактивації препаратів, змін фізичних показників готових ЛЗ, хімічної несумісності інгредієнтів у складі однієї лікарської форми. Поліморфні модифікації низки широко застосовуваних лікарських речовин різні за хімічною стабільністю, гігроскопічністю, механічними та фармакологічними властивостями, пресованістю. Залежно від типу зв'язків у кристалі, умов довкілля та хімічної структури вони можуть переходити в свої менш активні стабільні або нестабільні
форми (24).
Тести на визначення поліморфізму включені до вимог, розроблених Управлінням з контролю за харчовими продуктами і лікарськими препаратами США (FDA), щодо аналітичного контролю нових ЛЗ. Затверджено набір методик для виявлення і вивчення поліморфізму.
Розробку ЛЗ можливо поліпшити, якщо максимально вивчити всі фізичні параметри та корегувати їх з урахуванням вірогідних ризиків.
Вплив поліморфізму на фармакотехнологічні, біофармацевтичні та фармакокінетичні властивості лікарських речовин
Фізико-хімічні властивості кристалів обумовлюють здатність до пресування, сипкість, гігроскопічність, хімічну стабільність і біодоступність лікарських речовин.
Наприклад, кубічні кристали парацетамолу пресуються краще, ніж голчасті, що можна пояснити їхнім легким перегрупуванням, кращим контактом і більш міцними зв'язками. Різницю в гігроскопічності можна проілюструвати на прикладі лідокаїну* і тетракаїну, для яких втрата маси при висушуванні становить до 3,5 і 0,5% відповідно. Різниця в біодоступності обумовлює біофармацевтичну, а отже, і терапевтичну (клінічну) нееквівалентність хімічно ідентичних лікарських речовин. Наприклад, швидкість розчинення аморфної модифікації новобіоцину® (кислоти) в десять разів вища за таку її кристалічної форми. Саме тому в разі призначення обох форм новобіоцину® з розрахунку 12,5 мг/кг в
плазмі крові визначають тільки його аморфну модифікацію.
Різну біодоступність мають кристалічні поліморфні форми преднізолону.
У дослідах при імплантації форми І-фторпреднізолону атрофія кори надниркових залоз виникала в 1,5 разу швидше, ніж при застосуванні його d-моногідрату. Подібну ситуацію, безсумнівно, потрібно враховувати в клінічній практиці. Швидкість розчинення безводних форм кофеїну, теофіліну та глютетиміду значно вища, ніж їхніх сольватних форм. І навпаки, сольватні форми фторкортизонару і сукцинілфатіазолару розчиняються легше, ніж їхні несольватні форми. Гідрокортизону трибутил-ацетат у формі моноетанолсольвату
всмоктується в чотири рази швидше за його безводний аналог.
При тонкому подрібненні препарати краще розчиняються, швидше і повніше беруть участь у хімічних реакціях тощо. Подрібнення може істотно впливати на терапевтичну активність ЛЗ внаслідок зміни процесу їхнього всмоктування. Швидкість розчинення лікарських речовин прямо пропорційна площі поверхні, на якій відбувається всмоктування, і обернено пропорційна величині часток речовини.
Виявлено, що у разі призначення однакових доз сульфадимезидару, мікронізованого і отриманого в умовах заводського виробництва без додаткового подрібнення, в першому випадку в плазмі крові людей вміст речовини на 40% вище, максимальна концентрація досягається на 2 год раніше, а загальна кількість речовини, що всмокталася, на 20% більше,
ніж у другому випадку. Зменшення розміру часток ацетилсаліцилової кислоти до мікронізованих сприяє посиленню приблизно в два рази її анальгетичної, жарознижувальної і
протизапальної дії. Застосовуючи ту чи іншу поліморфну форму лікарської речовини, можна впливати не тільки на рівень абсорбції та фармакотерапевтичної активності препарату, а й змінювати тривалість його дії.

