Бикаш Чаттерджи, Участник экспертной панели CPhI WW, Президент и научный директор компании Pharmatech Associates
Создание фармацевтического производства будущего – настоящая гонка, в которой мощные рыночные тенденции формируют маршрут и правила на основе требований и вызовов «Фармы 4.0.» Мы находимся в преддверии масштабных изменений, вызванных ростом глобальных рынков, постоянной потребностью производителей фармацевтической продукции сохранять конкурентоспособность и неуклонно возрастающей сложностью работы, связанной со стремлением регулирующих органов осуществлять постоянный контроль за продукцией.
Экономическое развитие стран БРИК (Бразилии, России, Индии и Китая) расширило рыночные возможности и в то же время усложнило разработку и распространение безопасных и эффективных лекарств в глобальной цепочке поставок. Расходы на здравоохранение на душу населения должны возрасти с USD 1137 в 2017 г. до USD 1427 к 2021 г. Для многих эта тенденция неустойчива, и если отрасль не будет ориентироваться на сдерживание расходов при управлении эффективностью бизнеса, рынок может не досчитаться многих игроков.
Проблемы разработки лекарств
На данный момент фармацевтические компании находятся в постоянной гонке, борясь за ускорение инноваций и вывод новых лекарственных препаратов на рынок как можно быстрее и с минимальными затратами. Компании-новаторы считают, что их патентная защита подрывается, и, хотя патент может обеспечивать защиту интеллектуальной собственности компании в течение 20 и более лет, более половины этого времени будет потрачено на превращение идей, включенных в отдельный патент, в товарный продукт, оставляя только несколько лет, чтобы вернуть вложения, потраченные на разработку, величина которых нередко исчисляется миллиардами долларов. Добавьте к этому схему разработки, при которой рынка достигает только 13 % разработанных лекарств, и необходимость улучшения существующей модели станет абсолютно очевидной.
«Индустрия 4.0»: эволюция
Термин «Индустрия 4.0» был впервые использован федеральным правительством Германии в 2011 г. в национальной стратегии продвижения компьютеризированного производства. Обозначение «4.0» обыгрывало обозначение версий программного обеспечения и символизировало четвертый этап промышленной революции. Три предыдущие промышленные революции показаны на рис. 1 и описаны следующим образом:
• «Индустрия 1.0» относится к первой промышленной революции. Этап был отмечен переходом от ручного производства к станкам с использованием энергии пара и воды.
• «Индустрия 2.0» – это вторая промышленная революция, более известная как технологическая. Она стала возможной благодаря обширным железнодорожным сетям и телеграфу, что позволило быстрее перемещать людей и идеи. Этот этап был также отмечен возрастающим распространением электричества, что позволяло проводить электрификацию заводов и внедрять современные производственные линии. Это был период огромного экономического роста, сопряженного с повышением производительности.
• «Индустрия 3.0» состоялась в конце ХХ в., после окончания двух мировых войн, в результате замедления индустриализации и технического прогресса. Этот этап также называют цифровой революцией, поскольку он характеризуется широким использованием компьютерных и коммуникационных технологий в производственном процессе.
• «Индустрия 4.0» основана на появлении четырех технологий, которые разрушают привычный облик производственного сектора: стремительный рост объемов данных, вычислительной мощности и коммуникационных подключений, особенно новых глобальных сетей с низким энергопотреблением; появление аналитических и бизнес-аналитических возможностей; новые формы взаимодействия человека с машиной, такие как сенсорные интерфейсы и системы дополненной реальности; а также значительный прогресс в передаче цифровых инструкций в физический мир, примером чего могут служить продвинутая робототехника и 3D-печать.
«Фарма 4.0»
Цель «Фармы 4.0» – создать интеллектуальные ресурсы, необходимые инженерам и операторам для принятия более разумных решений, которые улучшают операционную эффективность, увеличивают доходность и производительность проектирования и, наконец, существенно повышают эффективность бизнеса. «Фарма 4.0» применяет концепции «Индустрии 4.0» к фармацевтической отрасли. На модульных структурированных интеллектуальных заводах киберфизические системы отслеживают физические процессы, создают виртуальную копию физического мира и помогают принимать децентрализованные решения. С помощью подключенных устройств Интернета вещей (IoT) киберфизические системы обмениваются информацией и взаимодействуют друг с другом и с людьми для контроля в режиме реального времени и сбора данных, которые вносят полезную информацию, поступающую затем к участникам общей цепочки создания стоимости. Концепции, помогающие таким образом повысить эффективность бизнеса, строятся на трех основных элементах:
• Широкое развертывание IoT: сбор данных во всей глобальной цепочке поставок с помощью интеллектуальных датчиков и интеллектуальных устройств.
• Инженерные системы: сбор данных и их обработка интегрированы для выявления, анализа и прогнозирования текущих и потенциальных производственных проблем.
• Интегрированный интеллект: «мозг» компании, где все данные, включая информацию от систем уровня целого предприятия, полностью взаимосвязаны во всей экосистеме.
Задачи «Фармы 4.0» амбициозны в том смысле, что ее целью является осуществление скачкообразного перехода от реактивной структуры, в которой исторически использовались стратегии и технологии автоматизации, к структуре прогнозирующей, основанной на аналитике и позволяющей предвидеть и решать потенциальные проблемы в общей цепочке поставок. И пусть фокус «Фармы 4.0» сосредоточен на производственной цепочке поставок, тем не менее принципы ее применяются гораздо шире, на протяжении всего жизненного цикла разработки лекарств.
Интернет вещей (IoT) и управление данными
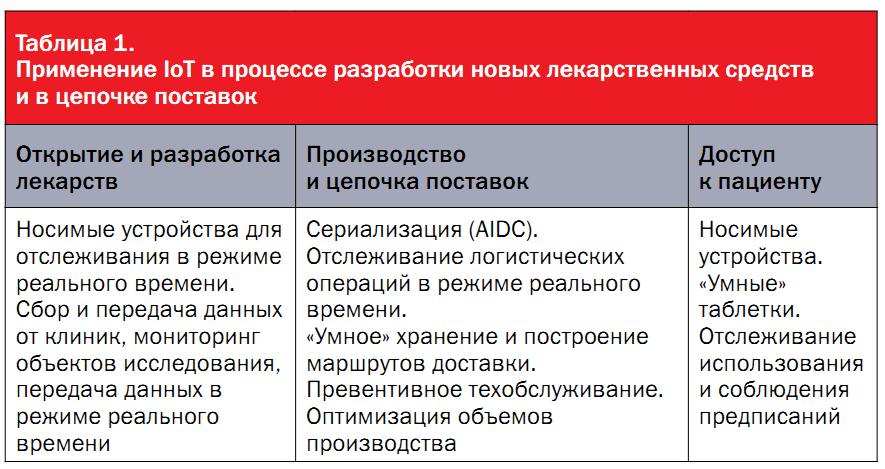
ІоТ – сфера, в которой вышеупомянутые принципы применяются еще начиная от стадии разработки лекарства. В приведенной ниже таблице 1 представлены некоторые из ключевых областей, в которых IoT используют в жизненном цикле разработки лекарств и в цепочке поставок, начиная от изобретения лекарства и заканчивая постпродажным фармаконадзором.
Прозрачность цепочки поставок остается очень большой проблемой для фармацевтической отрасли и сферы биотехнологий. Способность предвидеть сбои или осуществлять адресный надзор в режиме реального времени всегда была желанной целью. Как и любой процесс, цепочка поставок имеет свои уникальные сточники изменчивости. Независимо от того, является ли случившееся результатом влияния человеческого фактора или следствием механического отказа, способность отслеживать, измерять и, в конечном итоге, прогнозировать отклонения, которые не являются частью нормального управления процессом, требует возможности измерения параметров в реальном времени или практически в реальном времени. Сегодня решения IoT включают технологию сенсорных сетей в сочетании с интеллектуальным анализом данных. Соблюдение требований американского Агентства по контролю за качеством пищевых продуктов и лекарственных средств (FDA), предъявляемых к уникальному идентификатору устройства (UDI) FDA, и Закона о безопасности цепочки поставок лекарств (DSCSA) является важным фактором для развертывания IoT в цепочке поставок. Производители, включая владельцев регистрационного досье и контрактные производственные организации (CMO), должны были привести все в соответствие с законом к ноябрю 2018 г., что и так на год отставало от первоначальной цели. Соответствие закону определяли по внедрению на предприятии решения для генерирования уникального глобального номера позиции (GTIN), серийного номера, номера партии, даты истечения срока годности в удобочитаемом формате и кода матрицы данных, соответствующего GS1. Если рассматривать только рынок США, это серьезная техническая проблема, особенно с точки зрения управления базами данных. Если посмотреть на глобальный рынок и цепочку поставок, в которой существует более 70 различных стандартов и правил сериализации, то без труда можно заметить, что решения без комплексного подхода в долгосрочной перспективе окажутся нежизнеспособными.
Доступ к данным, разблокировка информации
Большая часть данных фармацевтической отрасли сегодня содержится в изолированных островках автоматизации и закрытых базах данных. Это было одной из первых проблем, с которыми столкнулась отрасль, пытаясь запустить анализ «больших данных» (Big Data Analytics). Разрозненные данные, собранные в обособленных, изолированных базах, значительно усложняют любой прогнозный анализ и серьезно ограничивают потенциал для любого нового и инновационного анализа. Если цель состоит в том, чтобы получить полный обзор всех соответствующих данных и их взаимосвязи друг с другом в контексте вашего бизнеса, пациентов, цепочки поставок и конвейера разработки, то нам нужна архитектура, которая может легко обрабатывать все типы данных. А разрозненные данные решить эту задачу не помогают. Интеграция данных оказалась самой сложной проблемой в ИТ, и существующие продукты и стратегии интеграции данных не работают. Большинство организаций имеют похожую архитектуру – набор операционных систем управления бизнесом, использующих комплекс инструментов извлечения, преобразования и загрузки (ETL) для подачи данных, чтобы обеспечить контроль за деятельностью предприятия.



