Марина Поліщук,
провідний спеціаліст відділу спектроскопії «АЛТ Україна»
ІЧ-Фур’є спектроскопія у фармацевтичній промисловості набуває дедалі більшої популярності як якісний та кількісний інструмент завдяки її неруйнівному характеру, легкій пробопідготовці та простоті використання для контролю складу сировини чи готової продукції. ІЧ-Фур’є спектроскопія також є найкращим вибором для мінімізації екологічних проблем, пов’язаних із промисловими хімічними відходами, оскільки не потребує великої кількості розчинника [1].
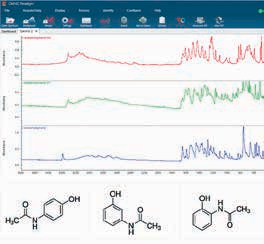
Рис. 1. Скриншот програмного забезпечення OMNIC™ Paradigm, на якому відображено різні ізомерні форми ацетамідофенолу
Компанія Thermo Fisher Scientific пропонує рішення для виконання рутинних завдань, таких як контроль якості згідно з Державною Фармакопеєю України (метод 2.2.24. Абсорбційна спектрофотометрія в інфрачервоній області), а також вирішення складніших задач, наприклад для аналізу ізомерів та поліморфів речовини або розподілу АФІ у лікарських засобах.
Дослідження ізомерних та полімерних форм ацетамідофенолу (парацетамолу)
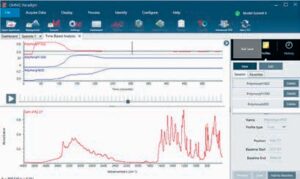
Рис. 2. Часова характеристика інтенсивності піків поліморфів ацетамідофенолу
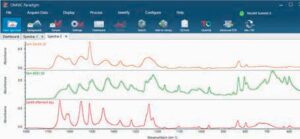
Рис. 3. Спектри трьох «кінцевих» поліморфів ацетамідофенолу, отриманих за різних умов. Спектр А відповідає аморфній формі ацетамідофенолу, спектр В — моноклінному поліморфу, спектр С — орторомбічному поліморфу
Як відомо, стереоізомери відрізняються фармакокінетичними та фармакодинамічними властивостями, тому можуть мати різне терапевтичне застосування та побічні ефекти, отже, їхнє вивчення є дуже важливим для розроблення рецептури фармацевтичного препарату [2].
В процесі дослідження було проведено експеримент із використанням ІЧ-Фур’є спектрометра ThermoScientific™ Nicolet™ Summit™ X ізDTGS детектором та програмним забезпеченням Thermo Scientific™OMNIC™ Paradigm, в якому невелику кількість зразка поміщали на аксесуар порушеного повного внутрішнього відбиття (ППВВ) ThermoScientific™ Everest™ з алмазним кристалом [3].
Було проаналізовано три ізомерні форми ацетамідофенолу. На рис. 1 представлено їхні спектри та відповідні хімічні структури. Кожен спектр було отримано за лічені секунди за допомогою аксесуара Thermo Scientific™ Everest™ із використанням лише незначної кількості зразка, що робить цей аналіз найбільш придатним для контролю якості сировини, а також кінцевих продуктів.
У фармацевтичних препаратах застосовують 4-ацетамідофенол, якому відповідає верхній спектр (рис. 1).
Відомо, що ефективність фармацевтичних препаратів значною мірою залежить від їхньої поліморфної форми, тому це важливий аспект, який слід ураховувати у процесі їхнього розроблення. Дуже важливо провести відповідний відбір для кожного АФІ та вибрати найбільш стабільний поліморф для розроблення та виведення на ринок продукту, щоб уникнути змін форми під час виробництва, доставлення або зберігання. Поліморфні перетворення у лікарській формі протягом терміну придатності, якщо такі відбуваються, не повинні суттєво
впливати на якість та біодоступність препарату [4].
У наступному дослідженні краплю ацетамідофенолу розчиняли в етанолі і наносили на ППВВ-приставку Thermo Scientific™ Everest™. За допомогою програмного забезпечення Thermo Scientific™OMNIC™ Paradigm знімали спектри із затримкою в часі в міру випаровування етанолу.
У початкових спектрах переважали піки розчинника етанолу. Приблизно через 10 хв від початку експерименту було отримано спектр сухого ацетамідофенолу. Протягом декількох хвилин спектр змінився на іншу форму, яка залишалася стабільною (рис. 2). Це пов’язано зі зміною морфології, спричиненою процесом сушіння. У верхній частині рис. 2 зображено зміну інтенси
вності характерних піків при 800, 1042 і 1500 см-1 для кожного з поліморфів із плином часу. Спектр, пов’язаний з поліморфом ph1042, показано у нижній частині рис. 2 [3].
Відомо, що одна й та сама молекула може кристалізуватися дещо по-різному на різних матрицях. Щоб дослідити цей ефект глибше, було проведено інший варіант аналізу з використанням ІЧ-підкладки.
Ацетамідофенол наносили на прозору для ІЧ-випромінювання поліетиленову мембрану, висихання якої відстежували за допомогою спектроскопії у режимі пропускання. Через кілька хвилин спектр стабілізувався з іншим профілем, який співставний з будь-яким із ППВВ-вимірювань. На рис. 3 показано результати всіх трьох експериментів: короткочасне ППВВ (початок досліду), довготривале ППВВ (через 10 хв після початку досліду) та пропускання (дослід із застосуванням ІЧ-підкладки). Результати пошуку та опубліковані дані літератури свідчать про те, що спектр А на рис. 3 відповідає аморфній формі ацетамідофенолу, спектр В —моноклінному полімо
рфу (форма I), спектр С — орторомбічному поліморфу (форма II).
У виробництві фармацевтичних препаратів застосовують ацетамідофенол в орторомбічній формі. Отже, спектрометр ThermoScientific™ Nicolet™ Summit™ у поєднанні із ППВВ-приставкою Thermo Scientific™ Everest™ є потужним інструментом для швидкого скринінгу, класифікації та аналізу ізомерів і поліморфів АФІ, таких як ацетамідофенол.
Дослідження розподілу АФІ за допомогою ІЧ-Фур’є мікроскопа
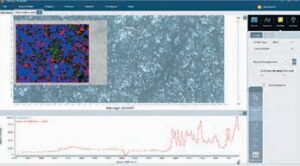
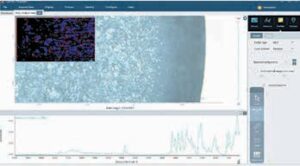
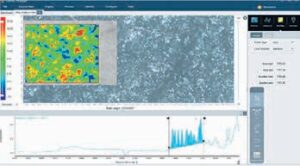
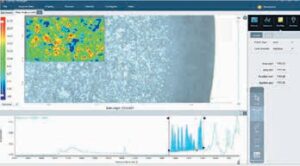
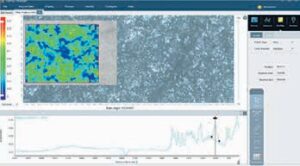
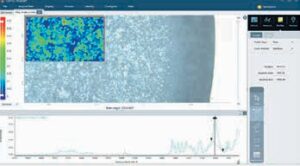
ІЧ-спектроскопію широко застосовують для візуалізації розподілу активних і допоміжних речовин. Розподіл різних компонентів (АФІ та допоміжних речовин) у матриці таблетки впливає на її твердість, міцність, властивості розчинення таблетки і вивільнення лікарського засобу. Для розуміння виробничих процесів і наслідків змін у визначеній матриці фармацевтичної рецептури важливо візуалізувати її склад та знати розподіл кожного інгредієнта. За допомогою традиційних спектроскопічних методів аналізу неможливо безпосередньо визначити просторовий розподіл компонентів у кінцевому продукті, саме тому в такому випадку застосовують підходи мапування та візуалізації [5]. ІЧ-Фур’є спектрометри Thermo Scientific™ у поєднанні з мікроскопом Thermo Scientific™Nicolet™ RaptIR™ забезпечують необхідні можливості та продуктивність як у візуальних, так і в ІЧ-операціях, дозволяючи новачкам і досвідченим користувачам отримувати корисні результати. У дослідженні було проаналізовано дві таблетки з ідентичними інгредієнтами в однакових концентраціях, щоб скласти мапу розподілу АФІ та допоміжних речовин. Спочатку було отримано високоякісні візуальні зображення таблеток (рис. 4). Програмне забезпечення Thermo Scientific™ OMNIC™Paradigm дозволяє автоматично отримувати зображення декількох ділянок, які становлять інтерес, в автоматичному режимі, навіть на окремих таблетках. У цьому випадку ІЧ-дані були зібрані за допомогою ППВВ-приставки з германієвим кристалом (контактний метод, що має дуже високе співвідношення сигнал/шум) із кроком 25 мкм для створення мапи ділянок розміром 1200 х 950 мкм на кожній таблетці. Для оброблення отриманих спектрів використовували метод MCR (з англ. MCR — Multivariate Curve Resolution), призначений для розкладання сумішей на окремі компоненти. MCR-зображення на рис. 4 і 5 двох таблеток показують розподіл трьох компонентів; компонент 1 позначений синім кольором, компонент 2 — зеленим, компонент 3 — червоним. Ділянки, позначені чорним кольором, є невизначеними трьома компонентами. Зображення MCR свідчить про значну різницю в тому, що таблетка 1 має більш однорідний розподіл компонентів порівняно з таким у таблетці 2.
Аналіз трьох складників засвідчив, що ацетамідофенол, натрію бікарбонат та крохмаль є інгредієнтами 1, 2 та 3 відповідно. Отже, за один цикл було визначено ідентичність, розподіл та відмінності у двох таблетках. На рис. 6 — 9 представлено специфічний розподіл ацетамідофенолу (див. рис. 6, 7) та крохмалю (див. рис. 8, 9) у двох таблетках.
В обох випадках таблетка 2 продемонструвала менший діапазон розмірів скупчень компонентів, що свідчить про різницю у виробництві таблеток (можливо, у процесі пресування або під час приготування двох препаратів), що видно навіть на візуальних зображеннях.
Таким чином, ІЧ-Фур’є мікроскоп Thermo Scientific™ Nicolet™RaptIR™ забезпечує чудові візуальні зображення (<1 мкм) та ІЧ-спектри з високою просторовою роздільною здатністю, а також набір потужних програмних інструментів для аналізу результатів. Широкий спектр застосування робить його ідеальним методом для використання у фармацевтичній галузі — від R&D до лабораторій контролю якості [6].
Рішення для аналізу фармацевтичних препаратів за допомогою ІЧ-Фур’є спектроскопії від компанії Thermo Fisher Scientific
ІЧ-Фур’є спектрометри ThermoScientific™ (рис. 10 — 12) є ідеальним рішенням як для рутинних, так і для дослідницьких завдань. Окрім описаних вище прикладів застосування, у поєднанні зі спеціалізованим програмним забезпеченням Thermo Scientific™ TQ Analyst™ вони також є ефективним інструментом для проведення кількісного аналізу [1].
Програмне забезпечення, за допомогою якого відбувається управління спектрометрами ThermoScientific™, відповідає всім вимогам 21 CFR, частина 11, та включає такі інструменти, як журнал аудиту, цифрові підписи, розмежування рівня доступу користувачів тощо.

Рис. 10. ІЧ-Фур’є спектрометрNicolet SummitХ
ТОВ «АЛТ Україна», офіційний дистриб’ютор рішень бренду Thermo Fisher Scientific в Україні
Тел.: +38 (044) 492-72-70
Spectroscopy@alt.ua https://alt.ua/
Список літератури
- MALLAH, Muhammad Ali, et al. A rapid Fourier-transform infrared (FTIR) spectroscopic method for direct quantification of paracetamol content in solid pharmaceutical formulations.Spectrochimica Acta Part A: Molecular and BiomolecularSpectroscopy, 2015, 141: 64 — 70.
- CHHABRA, Naveen; ASERI, Madan L.; PADMANABHAN, Deepak. Areview of drug isomerism and its significance. International journalof applied and basic medical research, 2013, 3.1: 16.
- OWRY, Stephen R.; SUKUMARAN, Suja. THERMO FISHERSCIENTIFIC. Application Note: Measuring isomers and polymorphsFeaturing the Nicolet Summit X FTIR Spectrometer. ApplicationNote, 2022.
- RAZA, Kaisar, et al. Polymorphism: The phenomenon affecting theperformance of drugs. SOJ Pharm Pharm Sci, 2014, 1.10.
- DOLE, Manjusha N., et al. Advance applications of Fourier transforminfrared spectroscopy. Int. J. Pharm. Sci. Rev. Res, 2011, 7.2:
159— 166. - THERMO FISHER SCIENTIFIC. Application Note: Rapid infraredmicroscopy in pharmaceutical product development, qualitycontrol and biologics formulation, 2023.