Без перебільшення, рекомбінантні реактиви, що приходять на зміну лізатам амебоцитів тваринного походження, відкривають нову сторінку в діагностиці ендотоксинів без участі тварин і мають низку переваг. Для українських фармацевтичних виробників вони теж доступні! ТОВ «Хімлаборреактив» («ХЛР») є офіційним представником Associates of Cape Cod, Inc. — піонера та вже 50 років як глобального лідера у виробництві продуктів та сервісів для визначення бактеріальних ендотоксинів і бета-глюканів. У статті наукові співробітники ДП «Український науковий фармакопейний центр якості лікарських засобів» (Харків) і фахівці компанії «ХЛР» розповідають про особливості й переваги новітніх реактивів.
Фармакопейне випробування лікарських засобів та медичних та медичних виробів у тесті in vitro на бактеріальні ендотоксини набуло офіційного визнання 1980 р., коли його вперше було внесено до Фармакопеї США 20-го видання. Метод аналізу бактеріальних ендотоксинів було розроблено на підставі відкриття Фредеріком Б. Бенгом (F.B.Bang) і Джеком Левіном (J. Levin) реакції згортання крові в найдавніших представників типу членистоногих із тих, які досі існують, — мечохвостів.
Причини розроблення реактивів із рекомбінантного білка
Використання мечохвостів, яких щорічно відловлюють у водах Атлантики в кількості приблизно 6 тис. для виробництва реактиву, негативно впливає на популяцію цього реліктового виду. Розуміння цього компанією Associates of Cape Cod Inc. (США), яка є найпотужнішим виробником реактивів для БЕТ, стало однією з причин розроблення нових реактивів із рекомбінантного білка на заміну наявному лізату тваринного походження.
Інша причина, яка виникає за використання будь-якого натурального інгредієнта, це значна варіабельність чутливості природного лізату, обумовлена, зокрема, статтю, віком, розміром мечохвостів, особливостями конкретного середовища їхнього життя й навіть сезоном і часом забору гемолімфи, а також активністю ферментної системи лізату, вираженість якої є генетичнодетермінованою.Природний лізат містить також багато інших білків, принаймні 10 з яких беруть участь в антимікробній відповіді й можуть або пригнічувати, або посилювати його коагуляційну активність.
Отримання й очищення лізату кожний постачальник здійснює в особливий спосіб: екстрагує складові хлороформом, залишає у ліофілізаті денатуровані білки, додає буферні розчини й детергенти, які є додатковим джерелом мінливості. Усе це впливає на чутливість отриманого реактиву до бактеріальних ендотоксинів і може стати причиною суттєвих відмінностей у результатах аналізу лікарських засобів. Тому існує думка, що рекомбінантні білки є більш стабільними, що дозволяє отримувати зіставні результати випробувань.
 Ще один недолік лізату біологічного походження — наявність у гемоцитах лізату альтернативного механізму активації процесів
Ще один недолік лізату біологічного походження — наявність у гемоцитах лізату альтернативного механізму активації процесів
гелеутворення через глюканчутливий фактор G (шлях фактора G). Протягом 10 років лізат амебоцитів Limulus використовували для контролю фармацевтичної продукції, перш ніж було зроблено приголомшливе відкриття — здатність інших матеріалів, а саме (1,3)-β-D-глюканів, які є компонентом клітинних стінок дріжджових та інших грибів, спричиняти хибнопозитивну реакцію, колибактеріальних ендотоксинів у препараті мало або взагалі немає.
Від клонування до комерційного виробництва
Ще в минулому сторіччі коагуляційна система мечохвостів стала очевидною, хоча й складною мішенню для зусиль генної інженерії. Вчені Національного університету Сінгапуру Дінг Джик Лінг (Ding Jeak Ling) і Хо Боу (Ho Bow) усвідомили потенціал, який може мати синтезований у лабораторних умовах рекомбінантний фактор С для розроблення технології виявлення ендотоксинів без тварин, і вже в 1995 р. клонували повнорозмірний фактор С, а в 1997-го — клонували й експресували рекомбінантний фактор С (rFC) у різних хазяїв. Науковці встановили, що за тих самих умов аналізу rFC має нижчі фонові показники й більш чутливу відповідь на ендотоксин порівняно з такими за використання комерційного ЛАЛ-реактиву.
Від клонування до комерційного виробництва рекомбінантного реактиву почалася нова ера швидкої кількісної діагностики ендотоксинів без участі тварин. Перший комерційний реактив на основі рекомбінантного фактора С для мікрофлуорометричного аналізу ендотоксинів був запропонований у 2004 р., пізніше з’явилися інші розробки. А у квітні 2021 р. Associates of Cape Cod., Inc.(США) спільно з японською компанією Seikagaku Corporation включила до лінійки комерційних пропозицій рекомбінантний каскадний реактив (rCR) PyroSmart NextGen™, клонований із генів мечохвоста Limuluspolyphemus, який подібно до його коагуляційної системи містить усі ферменти процесу коагуляції — фактори В та С і згортальний фермент разом із хромогенним субстратом, але виключає β-глюкан специфічний білок фактора G.
Таблиця 1. Порівняльний аналіз хромогенного кінетичного методу з PyroSmart NextGen®і лізатом амебоцитів за посиланням https://content.yudu.com/web/44k6f/0A44k6g/PIRApr25/html/index.html сторінка 63.
 Рекомбінантний реактив PyroSmart NextGen® дає змогу кількісно виявляти бактеріальні ендотоксини за допомогою хромогенного кінетичного методу, який є подальшою еволюцією гель-тромб- і турбідиметричного тестів. Хромогенний метод, елегантний за методологією, ґрунтується на кількісній залежності інтенсивності забарвлення реакційної суміші від концентрації ендотоксинів: що більше ендотоксину, то швидше фермент розщеплює субстрат — але не коагулоген, як у природі, а хромогенний паранітроанілін (pNA), що дає насичений жовтий колір (табл. 1).
Рекомбінантний реактив PyroSmart NextGen® дає змогу кількісно виявляти бактеріальні ендотоксини за допомогою хромогенного кінетичного методу, який є подальшою еволюцією гель-тромб- і турбідиметричного тестів. Хромогенний метод, елегантний за методологією, ґрунтується на кількісній залежності інтенсивності забарвлення реакційної суміші від концентрації ендотоксинів: що більше ендотоксину, то швидше фермент розщеплює субстрат — але не коагулоген, як у природі, а хромогенний паранітроанілін (pNA), що дає насичений жовтий колір (табл. 1).
Біотехнологічне виробництво PyroSmart NextGen® дає змогу отримувати стабільний від партії до партії продукт, чутливість якого до ендотоксинів не залежить від мінливості природних білків. Високу якість rCR підтверджують надійність і добра відтворюваність критеріїв придатності стандартної кривої та сталість параметрів реакції коагуляції.
Встановлено, щоPyroSmart NextGen® і лізат амебоцитів Limulus перевершують ефективність rFC до виявлення автохтонних ендотоксинів мікрофлори води, тому є найпоширенішою сировиною на фармацевтичному підприємстві.
 За результатами експериментальних досліджень, проведених компанією Associates of Cape Cod.Inc., встановлено, що реактив PyroSmart NextGen® виявляє певні переваги за умов тестування інтенсивно забарвлених розчинів порівняно з лізатами тваринного походження для хромогенного й турбідиметричного методів.
За результатами експериментальних досліджень, проведених компанією Associates of Cape Cod.Inc., встановлено, що реактив PyroSmart NextGen® виявляє певні переваги за умов тестування інтенсивно забарвлених розчинів порівняно з лізатами тваринного походження для хромогенного й турбідиметричного методів.
У дослідженні, виконаному М.Muroi (2019 р.), рекомбінантні реактиви PyroSmartтаrFCі 5 лізатів тваринного походження продемонстрували за ідентичних умов аналізу порівнянну реакційну здатність до ендотоксинів 13 різних штамів грамнегативних бактерій. Також не було зафіксовано істотних відмінностей у результатах аналізу 109 зразків парентеральних препаратів. Ба більше, рекомбінантні реагенти характеризувались від серії до серії помітно вищою відтворюваністю результатів, ніж лізати амебоцитів. На думку авторів, це достатньо переконливо демонструє, що рекомбінантні реагенти, зокремаPyroSmart, є дуже надійним інструментом, еквівалентним або навіть кращим за природний лізат амебоцитів, і придатним для рутинних випробувань ендотоксинів на фармацевтичному підприємстві.
Включено до провідних світових фармакопей
Аналіз ендотоксинів із використанням рекомбінантних реактивів поступово включають до провідних Фармакопей світу. З 1 січня 2021 р. в Європейській Фармакопеї набрала чинності загальна стаття Test for bacterial endotoxins using recombinant factor C» (2.6.32) з посиланням на флуорометричний метод визначення ендотоксинів із рекомбінантним фактором С. Того ж року у Фармакопеї Японії було опубліковано загальну інформацію щодо використання рекомбінантних реактивів (rCR) та (rFC) як альтернативних тестів (Bacterial Endotoxins Test and Alternative Methods using Recombinant Protein-reagents for Endotoxin Assay <G4-4-180>), де було зазначено, що аналіз ендотоксинів із деякими з рекомбінантних білкових реагентів виявляє однакову чи кращу чутливість і специфічність, ніж у методі з використанням реактивів лізату. Також як альтернативні розглядає ці методи USP у загальній статті <86> Bacterial endotoxins test using recombinant reagents, яка набуває чинності вже 1 травня 2025 р.
Таблиця 2. Параметри регресійного аналізу вмісту бактеріальних ендотоксинів із PyroSmart NextGen® і лізатом амебоцитів за посиланням https://content.yudu.com/web/44k6f/0A44k6g/PIRApr25/html/index.html сторінка 65.
У власних експериментальних дослідженнях оцінювали аналітичні характеристики (правильність, лінійність, прецизійність, діапазон застосування й межі кількісного визначення) відповідно до вимог загальної статті «Валідація аналітичних методик і випробувань» (5.3.N.2., ДФУ 2.4), Керівництва ICH Q2 та USP <1225>.
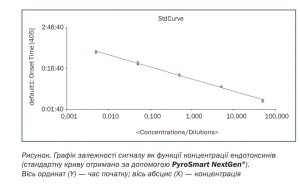
Дослідження проводили з використанням рекомбінантного реактиву PyroSmart NextGen® і стандартного препарату ендотоксину CSE (Escherichia coliO113:H10), які за посередництва компанії ТОВ«Хімлаборреактив» (Україна) були люб’язно надані фірмою-виробником Associates of CAPE COD, Inc. (США). В дослідженні застосовано хромогенний кінетичний метод у режимі on set time as say за довжини хвилі 405 нм на мікропланшетномуридері ELx808 виробництва компа-ніїBioTek Instruments Inc.(США). Яклізат амебоцитів використовували Pyrochrome®Associates of CAPE COD, Inc.(США). Аналітичні характеристики та критерії прийнятності випробування з використанням рекомбінантного реактиву PyroSmart NextGen® наведено в табл. 2. Стандартні криві для визначення ендотоксинів, отримані за допомогою PyroSmart NextGen®, задовольняли критерію надійності (|r|≥0,980) і дорівнювали 0,998–1,0 (рисунок).
Візуальна оцінка графіка залежності сигналу як функції концентрації ендотоксинів свідчить про наявність лінійної залежності (рисунок).
Як видно з табл. 2, відновлення до даного ендотоксину у відсотках від відомої концентрації до даних ендотоксинів задовольняє критерій прийнятності для перевірки факторів, що заважають, як описано в загальній статті ДФУ 2.6.14, тобто 50–200%. Діапазон становить 0,005–50 МО/мл, нижня межа кількісного визначення —0,005 МО/мл (табл. 2).
Короткі підсумки
Підсумовуючи дані наукових публікацій, інформаційно-довідкових матеріалів компанії Associates ofCape Cod. Inc., а також результати власних експериментальних досліджень, ми виявили низку переваг, які притаманні рекомбінантному реактиву (rCR) порівняно з лізатом амебоцитів тваринного походження, а саме:
• менша варіабельність реагенту від партії до партії, що підвищує внутрішньолабораторну співставність результатів і відтворюваність критеріїв придатності стандартної кривої;
• виключення хибнопозитивних результатів через індиферентність до (1,3)-β-D-глюканів та (1→4)-β-D-глюканів);
• вища реакційна здатність до Helicobacter pylori GU2 в експериментальних дослідженнях із використанням PyroSmartNextGen®, ніж в інших рекомбінантних реагентів (rFC), і суттєво нижчий заважаючий рівень впливу кальцію гепарину;
• виявлення переваг за умов аналізу інтенсивно забарвлених розчинів; • сприяння зменшенню використання тварин у фармакопейному контролі відповідно до положень 3Rs Європейської конвенції.
Як офіційний представник компанії Associates of Cape Cod в Україні «Хімлаборреактив» пропонує:
• повний асортимент реактивів і систем для проведення аналізу вмісту ендотоксинів;
• методичне підтримання, консультації з підбору оптимального рішення для вашого препарату (фахівці компанії «ХЛР» постійно проходять навчання на базі потужностей виробника);
• постачання з дотриманням належних умов перевезення й зберігання на сертифікованому складі.
Звертайтеся до компанії «Хімлаборреактив» www.hlr.ua,
аби отримувати найкращі рішення для контролю якості у фармацевтичній галузі!
Тетяна Леонтьєва, науковий співробітник лабораторії фармакопейного аналізу ДП «Фармакопейний центр», Харків
Юлія Меркулова, канд. біол. наук, провідний науковий співробітник лабораторії фармакопейного аналізу ДП«Фармакопейний центр», експерт Європейської Фармакопеї
Анна Журба, провідний фахівець відділу хімічних реактивів компанії «ХЛР»